Tag 1: Therapeutische Impfung, Gentherapie, Neue Medikamente, Plenary PL-1, 14.02.17
Jintanat Ananworanich, „The Emergence Potential for HIV Cure for Infants, Children and Adults“
Eine Eradikation des Virus kann nie bewiesen werden, also ist das naheliegende Ziel eine möglichst lange Remission. Das Reservoir wird in der frühen Phase der Infektion exponentiell aufgefüllt. Bei Neugeborenen besteht die Chance, extrem früh zu behandeln – mit einem entsprechend limitierten Reservoir. Doch selbst bei Patienten, die im Stadium Fiebig 1 behandelt wurden, steigt die Viruslast nach Absetzen der Therapie im Mittel nach 26 Tagen wieder an. Deshalb müssen zu einer frühen ART noch weitere Faktoren dazu kommen, z.B. „latency reversing agents“ (LRA), Immuntherapien und Gen- bzw. Zellbasierte Behandlungsformen. Wahrscheinlich aber sind Kombination erforderlich, so zeigen z.B. erste Versuche mit Therapeutischen Impfstoffen in Kombination mit LRA ermutigende Resultate. Immerhin dauerte es nach der Intervention und Absetzen der ART 9-12 Wochen, bis wieder Virus nachweisbar war. Ein weiterer Hoffnungsträger sind Breit Neutralisierende Antikörpber (bnAB), bzw. deren Kombinationen. Mit einer Kombination aus zwei dieser bnAB gelang es im Tiermodell, eine zwei Tage alte SHIV-Infekiton komplett auszuheilen.

Für eine Heilung von HIV wird wahrscheinlich ein Kombinationsansatz erforderlich sein
Carl H. June, “Advances in Cellular Therapy in Cancer and HIV”
Die Forschungen zu Krebs und HIV haben sich in den letzten Jahren gegenseitig befruchtet. Gen- bzw. Zelltherapeutische Ansätze spielen in beiden Gebieten eine zunehmende Rolle. So gelang die erste und bisher einzige Heilung eines Menschen von HIV nur mit gen- und zelltherapeutischen Methoden. Hinzu kommt, dass eine Fehlfunktion der CD4-Zellen bei beiden Krankheitsbildern eine entscheidende Rolle spielt. Auch der Einsatz von Immuntherapeutika wie z.B. PD1-Blockern wir hier wie dort geprüft. Ein besonder interessanter Ansatz sind T-Zellen mit „chimären Antigen-Rezeptoren. Normalerweise wird eine T-Zelle nur aktiviert, wenn ihr T-Zell-Rezeptor „sein“ Antigen erkennt und bindet. Nun ist es möglich, ein zusätzliches Gen für einen beliebigen Rezeptor einzuschleusen, so dass man die Zelle auf ein bestimmtes Aktivierungssignal „programmieren“ kann. Ein solches Signal kann ein Krebsantigen, aber auch ein Bestandteil von HIV sein. Bei einigen Krebsraten erreicht man mit diesen CAR-T-Zellen hohe Ansprechraten und die erste FDA-Zulassung einer darauf basierenden Behandlung wird noch 2017 erwartet. Da diese modifizierten T-Zellen oft jahrelang überleben, besteht auch die Möglichkeit einer lebenslangen Wirkung. Leider finden im Bereich HIV derzeit keine klinischen Studien mit dieser Methode statt, vermutlich wegen einiger Rückschläge in der Vergangenheit.
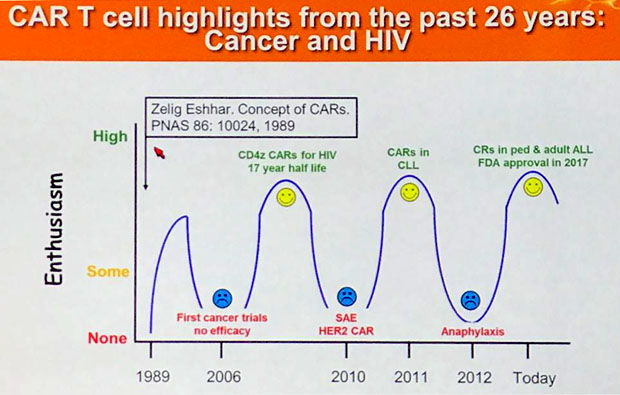
Bei der Entwicklung der CAR-T-Methode gab es immer wieder Euphorie und Rückschläge
Oral Abstract O-4: New HIV Drugs, Formulations, Combinations and Resistance
Abstract 38 Winston C. Tse, “Discovery of Novel Potent HIV Capsid Inhibitors with Long-Acting Potential
Gilead hat einen neuen Pfeil im Köcher: Mit dem oralen Capsid-Inhibitor GS-CA1 steht nach den Integrasehemmern erstmals wieder ein neuer Behandlungsansatz in den Startlöchern. Diese Substanz blockiert aber nicht nur den Zusammenbau des HIV-Capsids aus p24-Untereinheiten, sondern es blockiert irgendwie auch die nukleare Translokation, d.h. den Transport der viralen RNA in den Zellkern. Außerdem ist sie im picomolaren Bereich wirksam, hat eine sehr lange Halbwertszeit, die vielleicht einmal eine monatliche Dosierung ermöglicht und wirkt gegen alle HIV-Subtypen. In vitro gelang es zwar, resistente Viren zu züchten, doch diese Viren haben eine deutlich verringerte Fitness. Es wird sich lohnen, die weitere Entwicklung dieser Substanz(-Klasse) aufmerksam zu verfolgen.
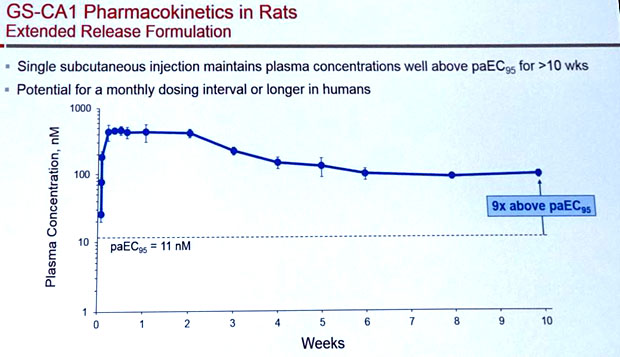
Die lange Verweildauer im Körper wird vielleicht eine einmal monatliche Gabe ermöglichen – momentan aber nur bei Ratten.
Abstract 39: Andrew Owen, “Human Confirmation of Oral Dose Reduction Potential of Nanoparticle Formulations”
Mit einer “Nanopartikel-Formulierung” ist es gelungen, antivirale Wirkstoffe wie Efavirenz oder Lopinavir so aufzubereiten, dass die halbe Dosierung ausreicht um vergleichbare Wirkstoffspiegel zu erreichen wie bei den zugelassenen Medikamenten. Gleichzeitig werden die Substanzen dadurch wasserlöslich, was z.B. die Verabreichung bei Kindern erleichtert.
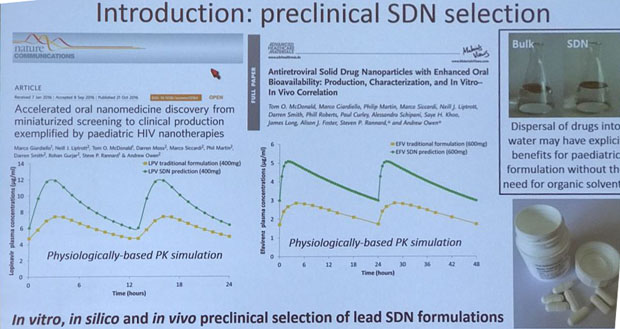
Medikamente in Nanoformulierung: Weniger Substanz und für Kinder geeignet.
Abstract 40 Joseph M. Custodio, “Clincal Pharmacology of the HIV Integrase Strand Transfer Inhibitor Bictegravir”
Bictegravir heißt der neue Integrasehemmer von Gilead, der nicht mehr geboostet werden muss. Er hat eine lange Halbwertszeit von 18 h und wird, wenig überraschend, gleich in Kombination mit TAF/FTC als „Single Tablet Regimen entwickelt“. Die Verstoffwechselung erfolgt über CYP 3A4 und UGT1A1 und nur wenn beide Enzymssysteme gehemmt werden, soll das einen relevanten Einfluss auf die Plasmaspiegel von Bictegravir haben.
Abstract 41 Paul E. Sax, “Randomized Trial of Bictegravir or Dolutegravir with FTC/TAF for Initial HIV Therapy”
Die nächste Arbeit vergleicht Bictegravir mit dem voraussichtlichen Hauptmitbewerber Dolutegravir. Wie nicht anders zu erwarten, sind beide Substanzen hoch wirksam und gut verträglich. Die Unterschiede sehen auf den ersten Blick minimal aus, die Marketingabteilungen der beiden Firmen werden sich anstrengen müssen, um Alleinstellungsmerkmale zu finden.
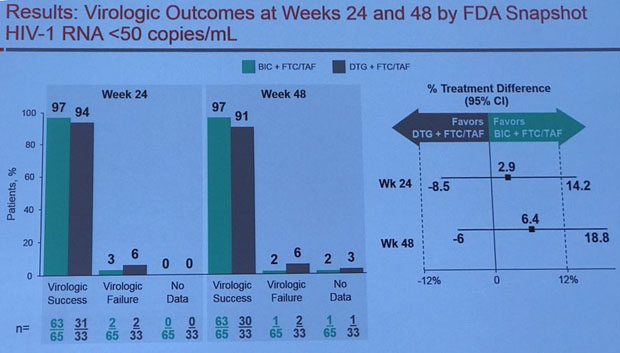
Bictegravir vs. Dolutegravir: Keine großen Unterschiede im direkten Vergleich
Abstract 42 José L. Blanco, “Pathways of Resistance in Subjects Failing Dolutegravir Monotherapy”
Dolutegravir wird zunehmend als Monotherapie eingesetzt, auch wenn es dafür keine großen Studien und schon gar keine Zulassung gibt. Und wie bisher bei jeder anderen Substanz treten auch unter Dolutegravir-Monotherapie Resistenzen auf. Dabei kann es auch zu einem Versagen kommen, wenn die Patienten schon lange eine Viruslast unter der Nachweisgrenze hatten und anscheinend eine gute Compliance aufwiesen. In drei großen Kohorten kam es bei etwa 9% der Patienten, die auf Dolutegravir Mono umgestellt wurden, zum Therapieversagen mit Resistenzentwicklung. Dabei sah man unterschiedliche Pfade (92Q, 118R, 148X und 155H).
Abstract 44LB Joseph M Llibre, “Phase III SWORD 1&2: Switch to DTG+RPV Maintains Virologic Suppression through 48 Wks”
Besser sieht es aus mit Zweifachkombinationen, z.B. Dolutegravir + Rilpivirin. In zwei Studien zeigte diese Kombination eine vergleichbare Wirkung wie die klassische Dreifach-Kombi. Auch die Verträglichkeit war gut und die Zweifachkombi erwies sich als lipidneutral.
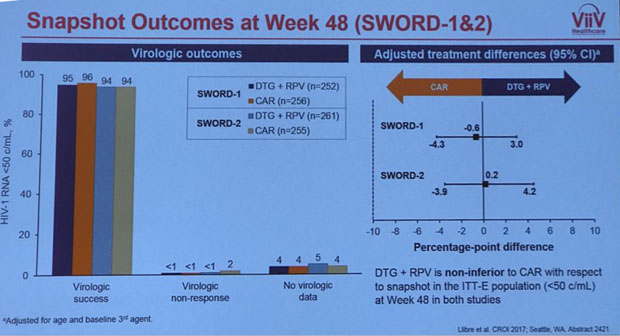
In beiden Studien war die Wirksamkeit von Dolutegravir + Rilpivirin vergleichbar mit einer Dreifachkombination („CAR“)
Abstract 45LB Kathleen Squires, “Doravirine is Non-Inferior to Darunavir/r in Phase 3 Treatment-Naïve trial at Week 48”
Doravirine, ein neuer NNRTI aus dem Hause MSD ist schon etwas länger bekannt. Nun musste er sich in einer Phase III-Studie mit dem Proteasehemmer Darunavir, geboostet mit Ritonavir, vergleichen (jeweils in Kombination mit 2 Nukleosidanaloga). Wie auch andere NNRTI (z.B. Efavirenz), zeigte sich Doravirine dem Proteasehemmer gegenüber als „nicht unterlegen“, auch bei hoher Viruslast. Die Verträglichkeit war gut und auch die Einflüsse auf den Stoffwechsel waren minimal.
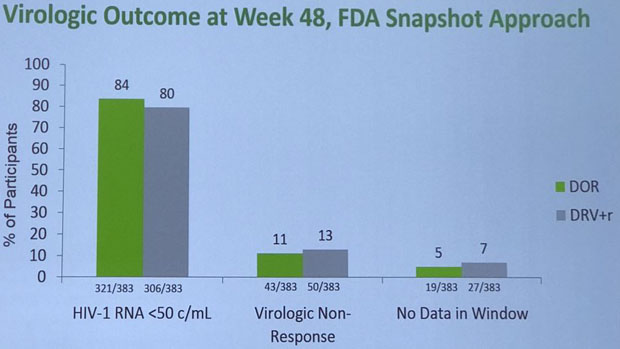
Doravirine vs. Darunavir/r (+ jeweils 2 Nukes): Ähnliche Wirksamkeit, ähnliche Verträglichkeit
Symposium S-1 Visions of HIV Cure
Diese Session, bestehend aus vier Präsentationen, war leider typisch für die CROI: Grundlagenforscher toben sich aus und das Auditorium versteht nur noch Bahnhof.
Deshalb hier eine Kurzzusammenfassung von dem, was ich glaube, verstanden zu haben:
Abstract 46 Daniel E. Kaufmann, „Visualizing Persistent HIV in Clinical Samples“
Soweit ich es verstanden habe, ging es darum, dass eine Färbung der Zellen nach RNA und Protein (gag) genauere Aussagen erlaubt als die Einzelfärbungen. Die Messungen werden dadurch bis zu 1000fach genauer.
Abstract 47 Mary F. Kearney, „Characterizing HIV Expression in vivo“
Vermehrt sich HIV, so macht es Fehler. Findet man unter der Therapie also sehr verschiedene HIV-Klone, deutet das auf eine weitergehenden Vermehrung von HIV hin. Findet man aber nur Kopien eines Klones, deutet das eher auf eine klonale Expansion hin, d.h. HIV-infizierte Zellen teilen sich und dabei wird das integrierte HIV an beide Tochterzellen weitergegeben. Außerdem ist auch nur eine Minderheit der integrierten Viren replikationskompetent.

Die Schlussfolgerungen sprechen für sich selbst, oder?
Abstract 48 Mirko Paiardini, “Immune-Based Interventions Targeting Inflammation and Viral Persistence”
Das Problem bei der HIV-Infektion besteht einerseits im latenten Reservoir, andererseits aber auch in der Immundysfunktion. Es ist also denkbar, dass auch bei einer Eradikation von HIV die Immundysfunktion nicht automatisch verschwindet. Für beide Erscheinungsformen der HIV-Erkrankung müssen also Lösungen gefunden werden. Soweit bin ich mitgekommen, danach bin ich ausgestiegen. Es ging um Möglichkeiten, die Immunaktivierung durch HIV zu verringern, z.B. durch IL-21 und IFNalpha, um ko-inhibitorische Rezeptoren wie CTLA-4 und PD-1 (bzw. deren Hemmung mit Antikörpern) und schließlich um Kombinationsstrategien.
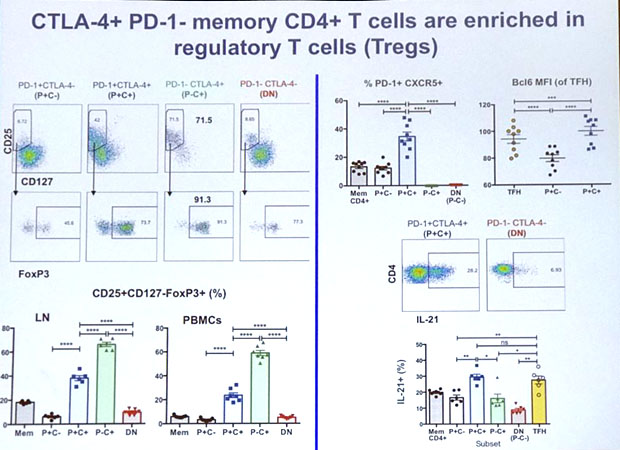
Das ist doch wirklich mal eine gelungene Darstellung...
Abstract 49 Louis J. Picker, “Therapeutic Vaccination for HIV/SIV: What will it take for a Cure?”
Obwohl nu rein Bruchteil des HIV-Reservoirs aus vermehrungsfähigen (replikationskompetenten) Viren besteht, ist dieses Reservoir doch so groß, dass bisher eine komplette Eradikation nicht funktioniert hatten. Deshalb wählten sich die Forscher ein Tiermodell mit einem viel kleineren Reservoir, nämlich Affen, die gerade erst wenige Tage infiziert waren. Diese Affen waren aber zuvor geimpft worden und zwar mit einem Konstrukt aus einem Affen-CMV-Virus und SIV-Proteinen. Bei diesen Affen vermehrt sich das Challenge-Virus zwar kurzfristig aber danach sinkt die Viruslast sofort wieder und nach einiger Zeit ist im ganzen Körper kein Virus mehr nachweisbar. Dafür gibt es zwei möglich Erklärungen: Entweder führt der Impfstoff zu einer Kontrolle und aktiven Elimination des ansonsten stabilen Reservoirs oder der Impfstoff stoppt lediglich die Vermehrung und das (noch instabile) Reservoir wird spontan abgebaut. Nach vielen (hochkomplizierten) Versuchen kam heraus:
Das Virusreservoir ist etwa bis zum Tag 5 nach Infektion instabil und kann, wenn die Vermehrung gestoppt wird, über die Zeit spontan eliminiert werden.
Etwa ab Tag 6 ist das Reservoir dann so stabil, dass es auch durch eine noch so lange suppressive Therapie nicht mehr spontan eliminiert wird.
Latent infizierte Zellen können über Monate hinweg ruhen, bevor sie aktiviert werden. Dabei reicht ein einziges solches Aktivierungsereignis aus um die Virusvermehrung erneut zu starten.
Im Vortrag wurde zwar nicht darauf eingegangen, aber wenn sich diese Ergebnisse auf den Menschen übertragen lassen, müssen wir u.a. auch das Konzept der Post-Expositions-Prophylaxe an diese Ergebnisse anpassen (d.h. ein PEP würde bis 5 Tage nach Exposition Sinn machen, aber ggf. müssten die Medikamente dann länger gegeben werden).
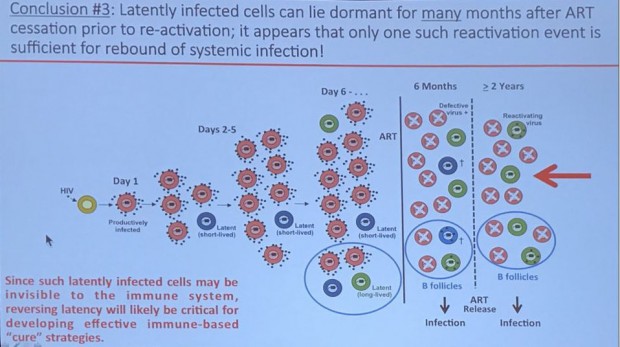
Wichtige Daten verpackt in anschauliche Bilder: Ab Tag 6 erfolgt keine spontane Elimination des Reservoirs mehr.