Nils Von Hentig, Frankfurt
Legal Highs und cART: Vorsicht Interaktionen!
Designerdrogen werden auch als Research Chemicals oder „Legal Highs“ bezeichnet, da sie aufgrund ihrer Neuheit (noch) nicht vom Betäubungsmittelgesetz erfasst sind. Der Bericht der Drogenbeauftragten der Bundesregierung Marlene Mortler vom Mai 2015, erwähnt 164 neue psychoaktive Substanzen, die zwischen 2005 und 2011 aufgetaucht sind. Synthetische Cannabinoide und synthetische Phenylethylamine/Cathinone machen seit 2005 zwei Drittel aller neuen Substanzen aus, die über das Frühwarnsystem gemeldet werden. Zudem gibt es auch vermehrt Meldungen über Substanzen aus eher seltenen chemischen Gruppen.
Nur scheinbar harmlos
Die für Missbrauchszwecke geeignete Wirkung der veränderten Substanzen auf die Psyche bleibt jedoch erhalten oder wird durch die chemischen Veränderungen sogar verstärkt. Die Drogen werden häufig als Kräutermischungen, Badesalze, Lufterfrischer oder Pflanzendünger verpackt und verkauft, ohne die wirklichen Inhaltsstoffe anzugeben. Da-bei wird der Eindruck vermittelt, sie seien ungefährlich und gesundheitlich unbedenklich. Tatsächlich aber zieht der Konsum teilweise schwere Folgen nach sich.
Europäische Webseite
| Substanz (engl.) | Jahr | name |
|---|---|---|
| 1-cyclohexyl-4-(1, 2-diphenylethyl) piperazine | 2014 | MT-45 |
| 4-methyl-5-(4-methylphenyl)-4, 5-dihydrooxazol-2-amine (4, 4′-dimethylaminorex, 4, 4′-dMAr) | 2014 | 4,4´-DMAR |
| 1-(1, 3-benzodioxol-5-yl)-2-(pyrrolidin-1-yl)pentan-1-one | 2014 | MDPV |
| 2-(3-methoxyphenyl)-2-(ethylamino)cyclohexanone | 2014 | Methoxetamin |
| 2-(4-iodo-2, 5-dimethoxyphenyl)-n-(2-methoxybenzyl)ethanamine | 2014 | 25I-NBOMe |
| 3, 4-dichloro-n-{[1-(dimethylamino)cyclohexyl]methyl} benzamide | 2014 | AH-7921 |
| 4-methylamphetamine | 2014 | Methamphetamin |
| 5-(2-aminopropyl)indole | 2014 | n.n. |
| mephedrone | 2011 | Mephedron |
| tMA-2 | 2004 | TMA-2 |
| 2C-i, 2C-t-2 and 2C-t-7 | 2004 | 2C…. |
| PMMA | 2003 | PMMA |
| gammahydroxybutyrat | 2002 | GHB |
| Ketamine | 2002 | Ketamin |
Tab. 1 Neuere Psychoaktive Substanzen, die ersten 6 Stoffe fallen 2014 nicht unter das BTM
Ein
genaues Bild der Substanzen liefert die Webseite des European
Monitoring Centre for Drugs and Drug Addiction
(EMCDDA).
Letztlich haben in den letzten Jahren vor allem sechs, nicht unter
das BTM fallende, Substanzen an größerer Bedeutung und Verbreitung
gewonnen. Alle neuen Stoffe finden
sich in Tab. 1, die ersten 6
Stoffe fallen derzeit nicht unter das BtMG.
Ketamin, GHB oder Metamphetamin ist der Mehrheit der Ärzte und Ärztinnen in der HIV-Therapie bekannt. Die neueren Substanzen, die in den letzten beiden Jahren neu auf den „Markt“ gekommen sind, werden sicherlich über kurz oder lang, auch Eingang in die Szene finden. Insbesondere lohnt sich den Blick auf: MT-45, 4,4-DMAR, MDPV, Methoxetamin, 25I-NBOMe und AH-7921.
MT-45
MT-45 (Szenename IC-6) wird typischerweise oral oder nasal appliziert, der Dampf der erwärmten freien Base kann inhaliert werden, das wasserlösliche Hydrochlorid-Salz kann i.v. injiziert werden. Die Einzeldosis beträgt 15-30 mg nasal, 25-75 mg oral. Die Einnahme einer weiteren Dosis wird oft berichtet. Die Effekte stellen sich etwa 15 min nach nasaler bzw. 60 min nach oraler Einnahme ein und halten ca. 2h an. Die Wirkung entspricht weitgehend anderen Opioiden, mit etwa dem 0.8-fachen der Wirkstärke von Morphin. User beschreiben beim Gebrauch keine Euphorie, eher Sedierung und eine potente analgetische Wirkung. (https://drugs-forum.com/forum/showthread.php?t=216091)
Es existieren keine Daten über die Pharmakokinetik von MT-45 und bisher wurde kein Metabolit des Stoffwechsels identifiziert. Eine Vielzahl von Studien im Tier haben gezeigt, dass sowohl das Racemat von MT-45 als auch die einzelnen (S)- und (R)-Enantiomere Opioid-Wirkung zeigen, wobei das (S)-Enantiomer mehrfach potenter als Morphin ist. In Rezeptor-Studien konnte nachgewiesen werden, dass MT-45 ein Opioid-Rezeptoragonist an den κ- und δ-Rezeptoren mit deutlich höherer Affinität als Morphin ist. Die akuten Nebenwirkungen liegen somit auf der Hand und betreffen vor allem Atemdepression und Obstipation. Maus-Studien zeigten darüber hinaus dauerhafte Konzentrations- und Lernschwierigkeiten nach chronischer Applikation, welche unabhängig von der Morphinwirkung zu sein scheinen. Die akute Toxizität von MT-45 ist um ein vielfaches Höher als die von Morphin, insbesondere bei i.v. Gabe.
4,4´-DMAR
Bisher würde von Europäischen Polizeibehörden ausschließlich das cis-Isomer als weißes oder farbiges Pulver bzw. in Tablettenform beschlagnahmt. 4,4´-DMAR findet sich häufiger als Zusatz in Ecstasy-Formulierungen. Die Applikation erfolgt oral, nasal und wie in einem Fall aus Ungarn berichtet auch als i.v.-Injektion. Typische Dosen bewegen sich zwischen 10-60 mg, in Einzelfällen würde über die Einnahme von 200 mg berichtet. Der Wirkstoff wurde ebenfalls als Verschnitt von Kokain im Straßenhandel gefunden.
Die Pharmakologie ist bisher nur in in-vitro-Studien erforscht und zeigte, dass 4,4´-DMAR in niedrigen Konzentrationen Dopamin (DA, EC50 8.6), Norepinephrin (NE, EC50 26.9 nM) und Serotonin (5-HT, EC50 18.5 nM) freisetzen kann. Pharmakodynamische Wechselwirkungen mit beispielsweise SSRI, MDMA oder Kokain sind wahrscheinlich sind. Insbesondere auf die Gefahr eines Serotonin-Syndroms wird hingewiesen. Hohe Dosen und/oder Kombinationen mit anderen Katecholamin-freisetzenden Substanzen im ZNS führen zu psychotischen Symptomen, Agitation sowie potenziell gefährlichen Kardiovaskulären Ereignissen durch Freisetzung von Norepinephrin in der Peripherie. Es existieren keine Daten zur Letalen Dosis von 4,4`-DMAR.
Konsumenten berichten bei der Einnahme von Euphorie, mentaler und physischer Stimulierung, empathischen Effekten sowie einer Veränderung der visuellen Wahrnehmung. Im Jahr 2014 wurden 31 Todesfälle im Zusammenhang mit der Einnahme von 4,4`-DMAR in Europa berichtet, insbesondere durch Hyperthermie, Krämpfe, Atemprobleme und Herzstillstand. Der vielleicht bekannteste Name im Straßenhandel für 4,4`-DMAR ist, chemisch nicht ganz korrekt, „Aminorex“.6-9
MDPV
MDPV (Szenenamen Flakka, Flex, Cloud Nine, Monkey Dust, MTV, Magic, Super Coke, Peevee) ist eines von über 50 Kationen. MDPV wird typischerweise als Pulver geliefert, welches in wasserlöslich i.v. oder s.c. appliziert werden kann. Es gibt ebenfalls Berichte über Kapsel-Tabletten und Lösungsformulierungen, sowie die rektale Applikation. Die üblichen Dosierungen sind 5-11 mg (Insufflation), 8-15 mg (oral) und 6-12 mg (rektal). Die erwünschten Wirkungen setzen etwa 5-30 min nach Applikation ein und dauern ca. 2-7h.
MDPV hemmt selektiv die Katecholamin-Wiederaufnahme (Dopamin Transporter (DAT) und Norepinephrin Transporter (NET), während der Serotonin-Uptake in diesem Fall wesentlich weniger betroffen ist. Die Effekte von MDPV halten im Tiermodel deutlich länger an als die von Kokain. Die Phase-1-Metabolisierung, schließen die Demethylierung, gefolgt von einer Methylierung, aromatischer Seitenketten-Hydroxylierung sowie Oxidation des Pyrrolidinrings zum korrespondierenden Lactam und Ringöffnung zur Carboxylsäure. MDPV wurde Mitte der 60er Jahre als ZNS-Stimulans u.a. in Deutschland patentiert. Bei Beschlagnahmungen wurde MDPV vielfach in Kombinationen mit Lidocain, Procain, Piracetam, Trimethoprim oder Diltiazem sowie Kokain, Ketamin, Methamphetamin, TFMPP, BZP, Mephedron, Methylone, 4-MEC, MDPBP, alpha-PVP und synthetischen Kannabinoid-Rezeptoragonisten gefunden. Informationen aus verschiedenen in-vitro- und in-vivo-Tierstudien zeigen eine Wirkung auf das Verhalten ähnlich dem von Kokain und Metamphetamin.
Der pharmakologische Schlüsselmechanismus ist die Blockade von Katecholamin-selektiven Transportern, wobei MDPV im Vergleich zu Kokain etwa 10-50mal potenter in der Hemmung ist. So erhöht MDPV beispielsweise in Ratten die Dopaminkonzentration im Nucleus accumbens. MDPV löst hierbei Tachykardie und Hypertonie sowie Hyperthermie aus.
CYP 2C19, CYP 2D6 und CYP 1A2 sind in der Verstoffwechselung von MDPV involviert. Es kann zu Wechselwirkungen mit anderen Medikamenten kommen, wie beispielsweise bei CYP 2C19/2C9: Fluoxetin, Carbamazepin, Moclobemid; bei CYP 2D6: Tramadol, Fluoxetin, Haloperidol, Diltiazem, Citalopram, Benzodiazepine; bei CYP1A2: Koffein, Diazepam, Cannabis, Olanzapine, Warfarin.
Die
typischen Wirkungen sind denjenigen von Kokain, Amphetaminen und
Mephedron vergleichbar. Nebenwirkungen schließen Tachykardie,
Hypertonie, Krämpfe, Schlaflosigkeit, Erbrechen, Bauchkrämpfe,
Schwitzen, Kopfschmerzen, reduzierten Appetit, erweiterte Pupillen,
Schwindel, Atemprobleme, Depression, Verwirrtheit, Agitation,
Aggression, Angstanfälle, auditive und visuelle Halluzinationen,
Gewaltausbrüche und paranoide Psychosen mit ein. Es liegen auch
einige Berichte über maligne Hyperthermie, Rhabdomyolyse,
Nierenversagen und Apoplexie vor. 108 Todesfälle wurden in der EU im
Zusammenhang mit dem Gebrauch von MDPV bisher registriert.
https://de.wikipedia.org/wiki/Methylendioxypyrovaleron).
Methoxetamin
Methoxetamin ist strukturell dem Ketamin vergleichbar. In den meisten Fällen wurde es als weißes (gelbes oder beiges) kristallines Pulver sichergestellt. Es wird als Pulver, Tabletten, Kapseln oder Lösung verkauft. Gewöhnlich wird Methoxetamin nasal insuffliert, oral eingenommen, kann aber auch als Salz in Wasser gelöst i.m. oder i.v. injiziert werden.
In einer bisher publizierten in-vitro-Studie wird gezeigt, dass Methoxetamin pharmakodynamisch affin zum NMDA (N-methyl-D-Aspartat) Rezeptor ist, also gleich Ketamin. Anders als Ketamin ist Methoxetamin aber ebenso affin zum Serotonin-Transporter. Die Wirkung ist ähnlich der von Ketamin, einem dissoziativen Anästhetikum: Diese sind Euphorie, Empathie, intensive sensorische Effekte, Dissoziation vom physischen Körper, Derealisation, Gefühle von Geborgenheit, vermehrte soziale Interaktion, Halluzinationen, Introspektion und kurzzeitige antidepressive Effekte.
Methoxetamin wird in Einzeldosen zwischen 10 und 200 mg eingenommen, auch wenn die Dosierung eigentlich 50 mg nicht überschreiten sollte. Die Wirkung stellt sich etwa 30-90 min nach nasaler, 90 min nach oraler und etwa 5min nach i.v. Applikation ein und halten für 1-7h an.
Das toxikologische Profil gleicht weitgehend dem des Ketamin. Methoxetamin wurde entweder alleine oder zusammen mit anderen Psychostimulanzien wie Lidocain, Phenacetin, und Koffein beschlagnahmt. Bisher wurden in der EU etwa 120 Fälle nicht-tödlicher Intoxikationen bekannt und etwa 20 Todesfälle werden im Zusammenhand mit der Einnahme von Methoxetamin berichtet.
Toxische Effekte sind u.a. Erbrechen, Diarrhoe, bradykarde Herzrhythmusstörungen, Bewusstseinsverlust, Schwitzen, Sehstörungen, Kopfschmerzen, Tremor, Desorientierung, Depression nach Abklingen der Wirkung, mentale Verlangsamung, Angst, sprach- und Bewegungsstörungen, Katatonie, Konfusion, Agitation, Aggression, Halluzination, Paranoia und Psychosen. Akute Intoxikationen gehen oft mit Agitation, Tachykardie, und Hochdruckkrisen einher. Ebenso gesehen wurden Ataxie und Nystagmus, was wiederum untypisch für eine Ketamin-Intoxikation ist.
Es gibt derzeit keine Daten über mögliche Wechselwirkungen mit Medikamenten, die z.B. den Arzneimittelstoffwechsel induzieren oder hemmen können. Dennoch ist klar, dass Methoxetamin mit anderen ZNS-wirksamen Depressiva, z.B. Alkohol die depressive Wirkung nach Gebrauch potenzieren und ebenfalls die Atemdepressive Wirkung verstärken können. Der gleichzeitige Gebrauch von Diazepam und anderen Benzodiazepinen erhöht die Plasma-Spiegel und reduziert die Clearance von Ketamin, so dass geschlossen werden kann, dass dies auch bei Methoxetamin möglich ist. Eine Konkurrenz um die Glukuronidierung könnte bei höheren Dosen mögliche Wechselwirkungen mit Morphinen und/oder Raltegravir/Dolutegravir bedingen. Das ist bisher jedoch nicht bewiesen, sondern nur ein möglicher Rückschluss aus den bisher bekannten Stoffwechselwegen.
Eine Veröffentlichung aus 2015 zeigt ebenfalls eine Rolle von CYP2B6 und CYP3A4 beim hepatischen Stoffwechsel von Methoxetamin, die möglichen Folgen einer Interaktion mit CYP3A4-Hemmern (Ritonavir, Cobicistat) sind jedoch bisher unklar, weil die potenzielle Wirkung der entstehenden Metaboliten nicht bekannt ist.
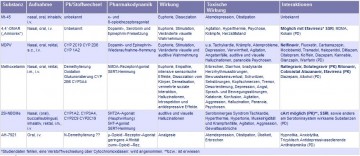
Tab. 2
Übersicht über Wirkungen und Pharmakologie sowie möglicher Wechselwirkungen (Pharmakokinetik, PK und Pharmakodynamik,
PD) der neueren Designerdrogen ![]()
25I-NBOMe
25I-NBOMe (Szenename: 2C-I-NBOMEe, 25I-N-Bomb) wurde in den frühen 2000er Jahren hergestellt. Die freie Base wird als farbloses Öl beschrieben und das Hydrochlorid-Salz ist ein weißes, wasserlösliches Pulver. 25I-NBOMe wurde typischerweise als Papier-Trips beschlagnahmt, d.h. absorbierendes Papier getränkt mit 25I-NBOMe für den sublingualen Gebrauch oder zum Auflegen auf die Zunge. Die typische Dosis bewegt sich zwischen 500 und 800 μg (sowohl für den oralen Gebrauch als auch die nasale Applikation) und die Wirkung setzt etwa nach 15-120 min ein und hält etwa 6-10h an.
25I-NBOMe ist ein voller 5-HT2A-Rezeptor-Agonist mit hoher Affinität zum Rezeptor in niedrigen nanomolaren Konzentrationen. Es produziert einen deutlichen und anhaltenden Effekt im HTR, welcher durch den 5HT2A-Rezeptorantagonisten Volinanserin aufgehoben werden konnte. Weitere Affinitäten von 25I-NBOMe wurden zu 5-HT1A/2B/2C, 5-HT6, Dopamin D3, D4, α2C Adrenorezeptor und dem Serotonin Transporter (SERT) gefunden.
Ein Screening der beteiligten Cytochromoxidasen zeigte die Beteiligung von CYP1A2, CYP3A4, CYP2C9/2C19 an der Metabolisierung. Auch eine Beteiligung von CytochromP450 erscheint möglich. Bisher würde keine letale Dosis für 25I-NBOMe angegeben.
Die Wege 25I-NBOMe einzunehmen sind vielfältig und schließen nasale Insufflation, buccale oder sublinguale Absorption der gelösten Substanz, i.v.- und i.m. Injektion sowie rektale Applikation und Rauchen mit ein. 25I-NBOMe wird heute als Ersatz für die illegal Droge LSD vertrieben und neuerdings werden auch Tabletten für den sublingualen Gebrauch hergestellt. 25I-NBOMe wurde bereits in unklaren Kombinationen mit anderen psychoaktiven Substanzen gefunden.
User beschrieben schwere psychische und Verhaltensänderungen, z.B. intensive auditive und visuelle Halluzinationen, schwere Agitation, Aggression und unvorhersehbare Gewaltausbrüche ein, die in einigen Fällen zu Traumata und Tod geführt haben. Klinische Fallberichte sprechen von serotoninergen Vergiftungserscheinungen sowie Agitation und Konfusion.
Interaktionen mit Medikamenten sind sehr schwer vorherzusagen, pharmakodynamisch ergeben sich jedoch sehr wahrscheinlich additive Toxizitäten zusammen mit anderen serotininergen Substanzen, wie z.B. SSRI und anderen Substanzen, welche die Serotoninkonzentration im ZNS anheben können und somit zum Serotoninergen Syndrom führen können. Symptome sind Tachkardie, Hyperthermie, Hypertonie, Muskelrigidität und Krampfanfälle.
AH-7921
AH-7921 (Szenename: Doxylam) ist ein strukturell atypisches synthetisches Opioidanalgetikum. Chemisch ist es ein Derivat von Hylaminocyclohexan. Das Hydrochloridsalz von AH-7921 ist ein weißer solider Stoff, wird aber auch als Pulver vertrieben. Ein anderer Name für AH-7921 ist „Doxylam” welches zum Teil mit Doxylamin verwechselt wird, einem international erhältlichen Generikum eines Antihistaminikums mit sedierenden und ebenfalls hypnotischen Eigenschaften, welches in verschreibungsfreien Antiallergika und Sedativa verwendet wird.
AH-7921 ist ein Morphin-ähnliches Analgetikum, welches hauptsächlich als μ-Opioid (MOP)Rezeptor-Agonist mit einer geringeren Affinität zum κ-Opioid (KOP) Rezeptor. Antagonisten sind beispielsweise Naloxon, ein typischer Opioid-Antagonist. Die analgetische Potenz liegt um ein Vielfaches über der von Kodein und ist etwa vergleichbar mit Morphin. Die analgetische Dosis liegt nahe am toxischen Bereich, so dass von einem sehr engen „therapeutischen“ Fenster auszugehen ist. Das Nebenwirkungsprofil ist vergleichbar dem von Morphin, wobei die atemdepressive Potenz in Tierstudien um etwa 1,6 über der von Morphin lag.
Scheinbar ist die orale Bioverfügbarkeit sehr gut, so dass AH 7921 oral und i.v. eingesetzt wird. Die von Usern berichten Dosen liegen zwischen 40 und 150mg, oftmals verstärkt durch mehrfache Dosierung im zeitlichen Abstand, damit der Effekt etwa 6-12h anhält. AH-7921 wird als „Recreational Drug“ eingesetzt, aber auch in Selbstversuchen als Analgetikum oder zur Substitution und Vermeidung von Entzugseffekten. AH-7921 hat in etwa dasselbe Abhängigkeitspotenzial wie klassisches Morphin. Bisher wurden 15 Todesfälle bis 2014 in der EU erfasst.
Über Interaktionen mit anderen Substanzen/Medikamenten gibt es keinerlei Erkenntnisse. Der sedierende Effekt wird aber sicherlich, wie bei Morphin auch, durch gleichzeitigen Gebrauch von Hypnotika, Anxiolytika, Trizyklischen Antidepressiva und sedierenden Antihistaminika gesteigert. Mittlerweile wird AH-7921 in einigen Ländern als illegal eingestuft: UK (Januar 2015; Brasilien Mai 2015, China Oktober 2015).
Weiterführende pharmakologische Informationen findet man auf der Webseite der EMCDDA:
www.emcdda.europa.eu/publications/drugs-in-focus/responding-to-new-psychoactive-substances








 Diese Seite weiter empfehlen
Diese Seite weiter empfehlen
