Akute HIV-Infektion
Die akute HIV-Infektion verursacht in 40 bis 90 % der Fälle vorübergehend Symptome. Dies geht mit einer hohen Vermehrungsrate von HIV und einer Virus-spezifischen Immunantwort einher.
Etwa ein bis vier Wochen nach der Infektion können körperliche Symptome auftreten, die aber nicht spezifisch für eine HIV-Infektion sind, sondern auch bei anderen Virusinfektionen (Erkältung oder Grippe, Pfeiffersches Drüsenfieber) auftreten.
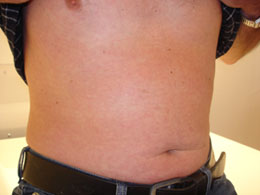
Hautausschlag bei aktuer HIV-Infektion
Symptome
Das häufigste Symptom ist Fieber. Zwischen 80 und 95% der frisch Infizierten entwickeln innerhalb des ersten Monats Fieber. Etwas seltener tritt eine Schwellung der Lymphknoten (Lymphadenopathie) an Hals und Nacken sowie in den Achselhöhlen auf. Gut zwei Drittel der frisch Infizierten (~70%) entwickeln eine Rachenentzündung (Pharyngitis) und einen Hautausschlag (Exanthem, siehe Foto). Der Ausschlag ist fleckig mit kleinen Knötchen (makulopapulös) und tritt hauptsächlich im Gesicht und am Körperstamm auf, seltener auch an den Extremitäten. Das Exanthem kann innerhalb von 24 bis 48 Stunden spontan wieder verschwinden. Selten kommt es zu einer geschwürigen (ulzerösen) Entzündung der Mundschleimhaut.
Gleichzeitig bestehen fast immer Allgemeinsymptome wie Abgeschlagenheit, Appetitlosigkeit (mit Gewichtsverlust), Kopf- und Muskelschmerzen (Myalgien). Selten kommen auch neurologische Erkrankungen vor, wie beispielsweise Entzündungen von Gehirn und/oder Hirnhäuten (Meningoenzephalitis, Meningitis), Nervenschmerzen der Extremitäten (periphere Neuropathie) oder Lähmungserscheinungen im Gesicht.
| Symptom | Häufigkeit |
|---|---|
| Fieber | 80 % |
| Hautausschlag | 51 % |
| Orale Ulzera | 37 % |
| Arthralgie | 54 % |
| Pharyngitis | 44 % |
| Appetitverlust | 54 % |
| Gewichtsverlust > 2,5 kg | 32 % |
| Allgemeine Abgeschlagenheit | 68 % |
| Myalgie | 49 % |
| Fieber und Hautausschlag | 46 % |
Die symptomatische Phase der akuten HIV-1-Infektion dauert 7-10 Tage, selten länger als 14 Tage. Den größten Voraussagewert für eine akute HIV-Infektion besitzt das gemeinsame Auftreten von Fieber und Hautausschlag innerhalb eines Monats nach einem adäquaten Risikokontakt.
Virus und Immunsystem
Während der akuten HIV-1-Infektion vermehren sich die Viren sehr schnell. Ohne die zu diesem Zeitpunkt noch nicht nachweisbare adaptive Immunantwort erreicht die Konzentration der HI-Viren im Blut (Viruslast) oft Werte von mehr als 100 Millionen Kopien HIV-1-RNA/ml. Es wird angenommen, dass während dieser Zeit wichtige pathogene Prozesse stattfinden. Dazu gehören die Aussaat der Viren in verschiedene Gewebe und die Zerstörung von T-Helferzellen (CD4-T-Lymphozyten) vor allem in Lymphgewebe und im Darm. Während der Rückbildung der Symptome werden HIV-spezifische Antikörper gebildet. Diese Antikörper werden im HIV-Test nachgewiesen.
Unmittelbar nach Bildung der HIV-Antikörper fällt die Viruslast deutlich ab und die T-Helferzellen steigen wieder an - zwischen Immunsystem und Virus ist es zu einer Art Gleichstand gekommen. Dieser wird nach spätestens sechs Monaten erreicht. Die Viruslast pendelt sich dann auf eine über längere Zeit stabile, individuell unterschiedliche Höhe ein (viraler Setpoint). Die Höhe des viralen Setpoint erlaubt eine prognostische Aussage über die Dynamik des weiteren Krankheitsverlaufes.
Diagnose
Eine schnelle Diagnose ist wichtig, denn wahrscheinlich werden etwa 50 % aller HIV-Neuinfektionen durch ebenfalls
frisch infizierte Patienten verursacht. Aber die akute Infektion wird oft nicht diagnostiziert, da andere virale
Erkrankungen ("Grippe" oder Pfeiffersches Drüsenfieber) für die Symptome verantwortlich gemacht werden. Zudem sind in
diesem frühen Stadium Antikörper meist nicht sicher nachweisbar.
Therapie?
Nicht endgültig beantwortet ist die Frage, ob es sinnvoll ist, bereits während der akuten HIV-Infektion mit einer antiretroviralen Behandlung zu beginnen - etwa, um irreparable Schädigungen des Immunsystems zu verhindern. Die Studienlage hierzu ist in den letzten Jahren reichhaltiger geworden, jedoch sind die Ergebnisse nicht eindeutig. Dennoch sprechen sich die meisten Leitlinien für eine sofortige Behandlung in dieser Situation aus. Selbstverständlich werden Patienten behandelt, die verstärkt unter den Symptomen einer akuten HIV-Infektion leiden.