Community Cure Workshop
2012 fand der erste „Cure Workshop“ statt, der von der Community organisiert wurde. Mittlerweile ist diese Veranstaltung Tradition und ein echtes Highlight, noch bevor die eigentliche CROI beginnt.
In diesem Jahr gab es zunächst eine kleine Einführung für Menschen, die nicht so mit dem Thema vertraut sind.
Anschließend sprach Hans-Peter Kiem über „Cell and Gene Therapy for HIV“. Da Teile seines Vortrags noch dem CROI-Embargo unterliegen, können hier (noch) nicht alle Details wiedergegeben werden.
Zunächst gab Kiem einen Überblick über den Fall von Timothy Brown sowie der beiden “Boston Patients” und berichtete, dass bisher alle weiteren Versuche, einen HIV-infizierten Menschen mit Hilfe einer allogenetischen Stammzelltransplantation mit CCR5-Delta32-Mutation zu heilen, gescheitert sind (6 Patienten starben an den Komplikationen der Prozedur). Man habe sich deshalb am Fred-Hutch-Center in Seattle (wo übrigens die Stammzelltransplantation entwickelt wurde) der autologen Stammzelltransplantation von genmodifizierten Zellen zugewandt. Dazu wird das „Next Generation Genome Editing“ eingesetzt, also Verfahren unter Einsatz von Zinkfingernukleasen, TALEN oder CRISPR/Cas9. Um eine Resistenz der Stammzellen gegen die HIV-Infektion zu erreichen, fokussiert man sich auf zwei Mechanismen: Disruption des CCR5-Rezeptors (hilft aber eben nur gegen R5-trope Viren) bzw. C46 Fusioninhibitor (Peptid abgeleitet von gp41 des Virus, wird auf der Oberfläche exprimiert und verhindert die Bindung sowohl von R5- als auch X4-tropen Viren an die Rezeptoren, eine Art endogenes T-20). Im Tierversuch schützt das C46-Peptid komplett vor einer Infektion der Zellen. Zwei Phase-I-Studien zu diesem Konzept bei Menschen mit HIV-Infektion und Lymphom beginnen soeben mit der Rekrutierung. Die komplette Prozedur – vom Ernten der Zellen über die Transduktion und die Vermehrung – kann inzwischen in einer einzigen Maschine, der CliniMACS Prodigy, durchgeführt werden. Fernziel sei aber die direkte Veränderung im Wirt durch eine entsprechende Genfähre bzw. ein therapeutisches Virus (funktioniert bereits für SCID bei Hunden).
Weitere Ansätze sind die Veränderung von Stammzellen so dass breit neutralisierende Antikörper gebildet werden können und die Produktion von Antikörper-ähnlichen Proteinen direkt in Muskelzellen.
Schließlich ging Kiem noch kurz auf die ersten Versuche mit CAR T-Zellen (Chimaeric Antigen Receptor T-Cells) ein.
Merlin Robb sprach über “MHRP (Military HIV Research Program) Studies in Early Treatment and the Journey towards Remission”.
Das MHRP führte zusammen mit dem Roten Kreuz in Thailand zwei groß angelegte Studien zur akuten Infektion durch. In der einen (RV217) testeten sich MSM mit hohem Risiko zweimal pro Woche selbst mit einem kombinierten Ag/Ak-Test. Bei einem positiven Ergebnis und Einwilligung der Patienten wurde dann sofort eine Therapie eingeleitet. Bei Patienten, die keine Therapie wollten, wurde der natürliche Verlauf beobachtet. In der zweiten Studie erhielten die Patienten sofort eine Kombinationstherapie, die noch um Maraviroc ergänzt wurde, um die Viruslast möglichst schnell zu senken:
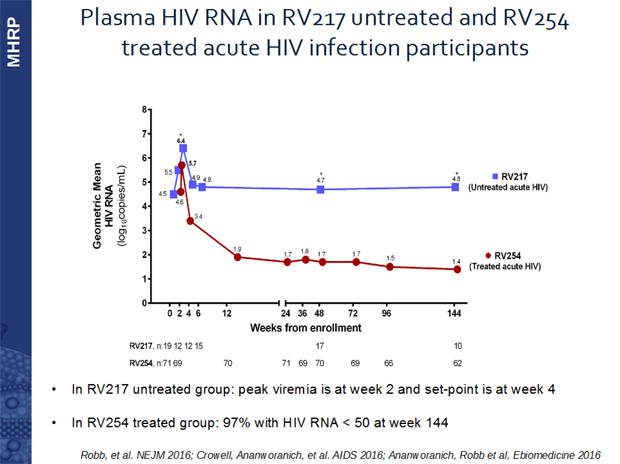
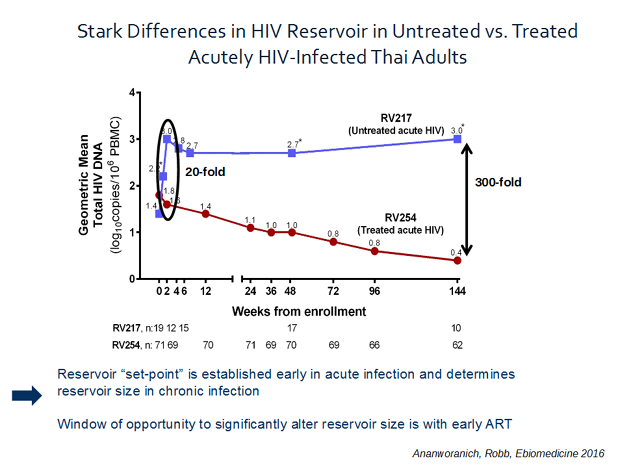
Schon zum Zeitpunkt der höchsten Viruslast („peak viremia“) war das Virusreservoir in der unbehandelten Gruppe um den Faktor 20 größer als in der behandelten. Nach 144 Wochen hatte sich dieser Unterschied weiter vergrößert: Bei Unbehandelten war das Reservoir nun um den Faktor 300 größer! Falls man also einen Patienten mit sehr früher HIV-Infektion entdeckt (Fiebig < IV), kann mit einer sofort eingeleiteten Behandlung die Reservoirgröße begrenzt werden. Dabei gilt es zu beachten, dass etwa 60% der Patienten, die in den ersten zwei Wochen nach Infektion behandelt werden, keine oder nur eine transiente Antikörperantwort entwickeln, sie also im HIV-Test negativ bleiben bzw. wieder werden. (Dies war für diese Menschen in Thailand, die z.T. Arbeit in arabischen Ländern mit obligatem HIV-Test suchten, von entscheidender Bedeutung!)
Bei einer Therapiepause zeigt sich ein signifikanter Unterschied zwischen früh und erst später behandelten HIV-Patienten: Bei früh behandelten (Fiebig < IV) kommt es zwischen 21 und 77 Tagen zum Wiederanstieg der Viruslast, bei später behandelten schon nach nur 5-29 Tagen. Doch obwohl dieser Unterschied signifikant ist, hat er derzeit keine klinische Bedeutung, könnte aber bei zukünftigen Eradikationsstudien bedeutsam sein.
Um die Größe des latenten Virusreservoirs weiter zu verringern, untersucht das MHRP zusätzliche Strategien:
Vorinostat als „latency reversing agent“
Einen Ad26/MVA-Impfstoff
Einen breit neutralisierenden Antikörper (VRC01)
Telmisartan als antientzündlichen Wirkstoff
Sowie verschiedene Kombinationen aus den o.g.
In Affen gibt es dabei schon erste Ergebnisse:
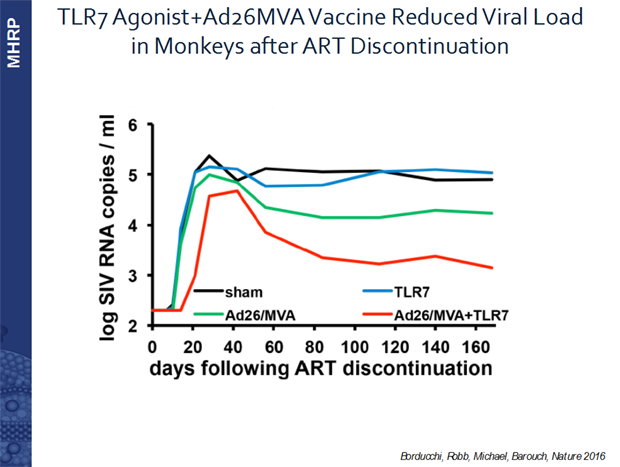
Davey Smith sprach über: “The last gift: Cure research at the end of life”
Dabei geht es um die Idee, zunächst rein beobachtende aber später auch interventionelle Studien an Menschen durchzuführen, die nicht notwendigerweise HIV-infiziert sind, aber eine terminale Erkrankung mit einer Lebenserwartung von weniger als sechs Monaten haben. Was zunächst makaber klingt, ist die Folge einer Interviewserie mit solchen Menschen, die ihr Sterben als zutiefst sinnlos empfinden und durch eine Studienteilnahme genau einen solchen Sinn sehen und darin Trost und Befriedigung finden.
Der große Vorteil wäre, dass man schnelle Autopsien (der zunächst gebrauchte Begrif „warme Autopsie“ wurde bald wieder verworfen) machen könnte, d.h. nur wenige Stunden nach dem Tod. Dies ist erforderlich, wenn man RNA analysieren möchte (wie z.B. von HIV), da diese extrem schnell degradiert. Interessanterweise würde sich ein erheblicher Teil dieser Patientengruppe sogar mit Nebenwirkungen abfinden und sogar mit Erregern infizieren lassen, wenn damit der Forschung geholfen wäre.
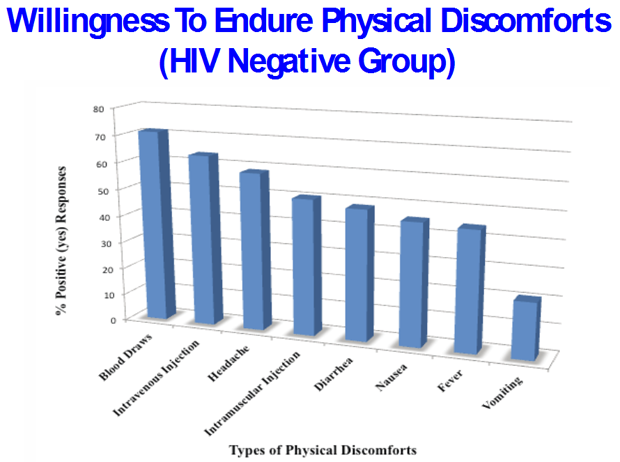
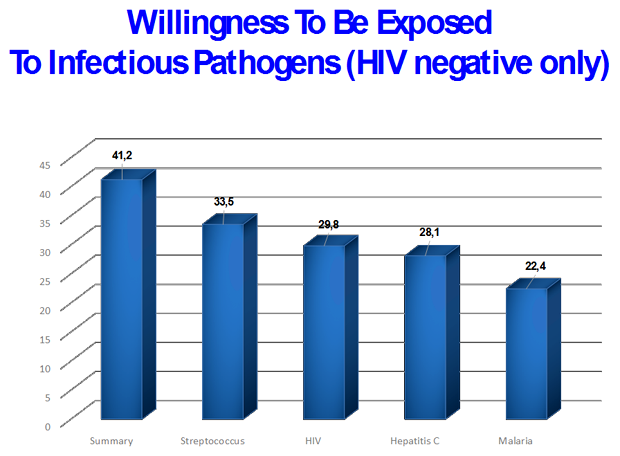
Inzwischen wurde eine erste Gruppe von 12 terminal Kranken identifiziert, die großes Interesse an einer Studienteilnahme haben. An diesen Probanden soll zunächst die genaue Verteilung des HIV-Reservoirs in den Geweben untersucht werden.
Schließlich sprach Eileen Scully über “HIV reservoirs in women“
Zunächst führte Scully aus, dass es – je nach Krankheitsbild – teilweise erhebliche Unterschiede zwischen den Geschlechtern gibt. Auch das Ansprechen auf Impfungen kann sich deutlich unterscheiden.
Als Gründe für die Unterschiede speziell bei der HIV-Infektion nannte sie u.a.
unterschiedliche Expressionsmuster von X-chromosomal codierten Genen (TLR7, FOXP3)
Unterschiede im Mikrobiom (z.B. des Darms aber auch des Genitaltrakts)
Direkter Einfluss von Östrogen, da die LTRs von HIV eine Östrogen-Bindungsstelle aufweisen
Dies führt dazu, dass die Viruslast und die Größe des latenten Reservoirs bei Frauen im Durchschnitt niedriger liegt. Leider ist dies nicht allen Forschen bekannt und so gibt es z.B. immer noch tierexperimentelle Studien, bei denen das Geschlecht der Versuchstiere nicht berichtet wird.
Bei Reaktivierungsstudien kann man T-Zellen durch Stimulation des T-Zell-Rezeptors (TCR) zur Produktion von Viren anregen. Diese Stimulation kann bei Frauen durch Gabe von Östrogen komplett unterdrückt werden, bei Männern nur zum Teil.
Ein Problem von in-vitro-Studien ist, dass der Indikatorfarbstoff, der für Zellkulturmedien verwendet wird, selbst eine östrogen-ähnliche Wirkung hat!
Bei Studien mit Menschen müssen in Zukunft nicht nur die geschlechtsspezifischen Unterschiede berücksichtig werden, sondern auch, ob die Frauen postmenopausal sind und ob sie östrogenhaltige Kontrazeptiva bzw. Hormonersatztherapie verwenden (im Falle von Trans-Frauen sogar in sehr hoher Dosierung).