Deutsche Patienten bitte hinten anstellen!
Ende
letzten Jahres wurde in Europa die Fixkombination
Darunavir/Cobicistat (Rezolsta®)
zugelassen. In den meisten europäischen Ländern wird das Medikament
auch eingeführt werden, nicht jedoch in Deutschland. Gleiches gilt
vermutlich auch für die Fixkombination Atazanavir/Cobicistat, die
kurz vor der europäischen Zulassung steht. HIV&more ging der
Frage nach, warum deutsche Patienten nicht in diesen Genuss kommen.
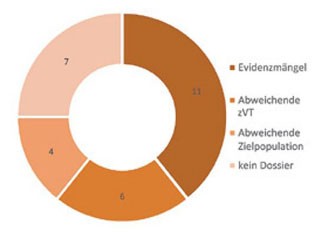
Abb. 1 Ausschlaggebende Gründe für fehlenden Zusatznutzen aus Sicht des G-BA 2011-2013 (n=28)
Seit 2011 werden gemäß AMNOG (Arzneimittelneuordnungsgesetz) Pharmahersteller aufgefordert für alle neuen Arzneimittel ein Nutzendossier entsprechend den Vorgaben des G-BA vorzulegen und dadurch einen patientenrelevanten Zusatznutzen gegenüber einer zuvor festgelegten zweckmäßigen Vergleichstherapie nachzuweisen. Danach verhandeln der GKV-Spitzenverband einen neuen Preis, d.h. einen Rabatt auf den zuvor vom Hersteller frei festgelegten Abgabepreis. Hersteller können diesen Prozess umgehen, indem sie das Dossier gar nicht, verspätet oder unvollständig einreichen. Oder der Hersteller zieht das Medikament aus dem Markt zurück – oder führt es erst gar nicht ein.
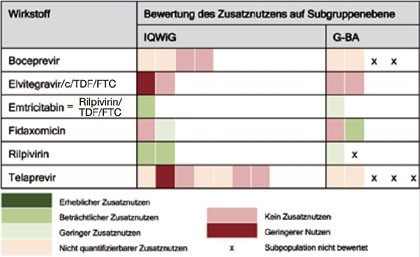
Abb. 2 Abweichungen des G-BA von der Bewertung des Ausmaßes des Zusatznutzens durch das IQWiG 2011-2013
AMNOG Bilanz 2011-2013
Bis Ende 2013 wurden 64 Nutzenbewertungen abgeschlossen und 44 Erstattungsbeträge vereinbart. Der G-BA hat dabei in 50% der Verfahren einen Zusatznutzen anerkannt. Gründe für den fehlenden Zusatznutzen waren nur bei rund einem Drittel der 28 Bewertungen ohne Zusatznutzen „Evidenzmängel“ (Abb. 1). In der Infektiologie haben bis Ende 2013 sechs Wirkstoffe die Nutzenbewertung durchlaufen (Abb. 2).
Unternehmer für Anfänger
Stellen Sie sich vor, Sie sind Hersteller von Produkt A, das obligat zusammen mit Produkt B einer anderen Firma angewandt werden muss. Ihr Produkt A kostet 5,- Taler und verkauft sich gut. Nun haben Sie eine Fixkombination A/C entwickelt, bei der die zusätzliche Anwendung von Produkt B entfällt. Einziger Vorteil Ihrer neuen Fixkombination ist die einfachere Anwendung. Den Preis für die neue Fixkombination A/C bestimmen aber Sie nicht allein. Der Preis wird nach festgelegten Spielregeln bestimmt, die aller Wahrscheinlichkeit nach zu einem geringeren Preis als 5,- Taler führen werden. Was werden Sie tun? Das neue Produkt A/C so schnell wie möglich auf den Markt bringen, auch wenn der Verkauf von Produkt A dann deutlich zurückgeht? Oder A/C nicht auf den Markt bringen?
 Anfrage bei
Bristol-Myers Squibb zu Atazanavir/Cobicistat
Anfrage bei
Bristol-Myers Squibb zu Atazanavir/Cobicistat
Eine Fixdosis-Kombination von Reyataz®/Cobicistat befindet sich in der EU in einem laufenden Zulassungsverfahren. Der Ausgang von Zulassungsverfahren ist nicht vorhersehbar. Wir bitten um Verständnis, dass wir zum jetzigen Zeitpunkt keine weiteren Informationen geben können. Die beiden Substanzen Atazanavir und Cobicistat sind einzeln bereits auf dem Markt verfügbar. Somit steht die freie Kombination bereits heute Patienten zur Verfügung.
 Kommentar
Gilead Sciences zu Vitekta® (Elvitegravir)
Kommentar
Gilead Sciences zu Vitekta® (Elvitegravir)
Gilead verpflichtet sich, Vitekta® allen Patienten der Europäischen Union zugänglich zu machen. Vitekta® ist nur indiziert zur Therapie von vorbehandelten Erwachsenen als Teil einer HIV-Kombinationstherapie, die einen mit Ritonavir geboosterten Proteasehemmer enthält. Angesichts dieser limitierten Indikation und anderen verfügbaren antiretroviralen Medikamente für vorbehandelte Patienten, stellt Gilead Vitekta® allen EU-Ländern zur Verfügung durch Importe über Großhändler und internationale Apotheken. Der Preis basiert auf den österreichischen Erstattungskosten. Für weitere Informationen stehen Ärzten die lokalen Gilead-Vertretungen zur Verfügung.










 Diese Seite weiter empfehlen
Diese Seite weiter empfehlen
