HIV-PEP - Berufliche Exposition
Aktuelle Beiträge zum Thema:
Ärztesuche: HIV-Schwerpunktpraxen
Sofortmaßnahmen
Nach jeder HIV-Exposition sollen zunächst die folgenden Sofortmassnahmen unverzüglich (in Sekunden) in der nachfolgenden Reihenfolge eingeleitet werden (ggf. kann anschliessend an die Sofortmassnahmen telefonisch weiterer Rat eingeholt werden):
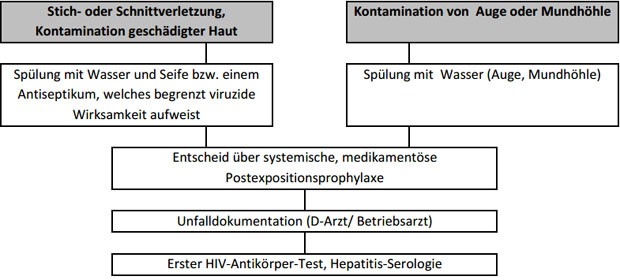
Stich-/Schnittverletzung
- Spontanen Blutfluss nicht sofort unterbinden, da potentiell infektiöses Material dadurch ausgespült wird.
Sonstige Manipulationen an der Wunde nach Möglichkeit vermeiden, insbesondere Quetschen und Ausdrücken direkt im
Einstichbereich, um keine Erregerverschleppung in tiefere Gewebsschichten zu begünstigen.
- Nach der spontanen oder induzierten Blutung ggf. Stichkanal bzw. Schnittverletzung spreizen und Spülung mit
Wasser/Seife oder Antiseptikum (z. B. Betaseptic® oder anderes Händedesinfektionsmittel oder Hautantiseptikum auf Basis
von Ethanol) durchführen.
Kontamination von Auge oder Mundhöhle:
Spülung mit nächst erreichbarer
geeigneter Flüssigkeit, d. h. in der Regel Leitungswasser
- Hautexposition (geschädigte oder entzündlich veränderte Haut): Gründliches Waschen mit Wasser und Seife. Danach, falls verfügbar, Abreiben der Hautoberfläche mit großzügiger Einbeziehung des Umfelds um das kontaminierte Areal mit einem mit Hautantiseptikum satt getränkten Tupfer.
- Kontamination des
Auges:Unverzüglich reichliches Ausspülen des Auges mit Ringer-, Kochsalzlösung oder Wasser.
- Aufnahme in die Mundhöhle: Sofortiges, möglichst vollständiges Ausspeien des aufgenommenen Materials. Danach mehrfaches Spülen (ca. 4-5 mal) der Mundhöhle mit Wasser. Jede Portion ist nach etwa 15 Sekunden intensiven Hin- und Her-Bewegens in der Mundhöhle auszuspeien.
Im Anschluss an die Sofortmaßnahmen legt der D-Arzt das weitere Prozedere bzgl. Schutzimpfung (Tetanus- und
HBV-Impfschutz, ggf. weitere), HIV-PEP und serologischer Untersuchungen (AK gegen HIV und HCV, ggf. weitere) im
Einverständnis mit dem Betroffenen fest.
Infektionsrisiko
Das Abschätzen des Infektionsrisikos ist notwendige Voraussetzung für eine rationale Entscheidung, d. h. für einen
kalkulierten Einsatz der medikamentösen Prophylaxe.
Das durchschnittliche Risiko einer HIV-Infektion nach perkutaner Exposition mit Blut von HIV-Infizierten, die eine
messbare Viruslast aufweisen, liegt nach den bisher vorliegenden Daten bei etwa 0,3 %; d. h. im Mittel führt eine von
330 Expositionen zu einer HIV-Infektion [70].
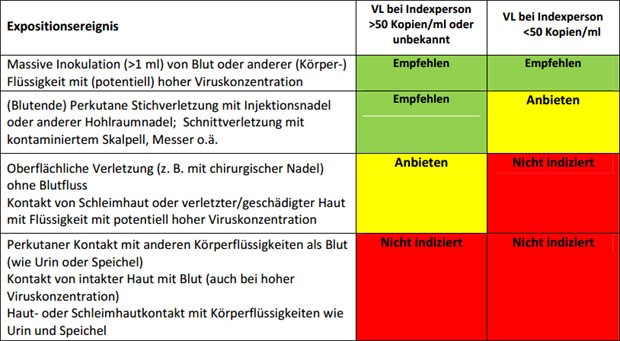
Ein gegenüber dem durchschnittlichen Risiko erhöhtes Infektionsrisiko im individuellen Fall besteht nach Analyse der Verletzungs- und Expositionsarten unter den in Tabelle 1 genannten Bedingungen. Das durchschnittliche Infektionsrisiko bei Schleimhautexposition und bei Exposition entzündlich veränderter Hautpartien liegt hingegen um 0,09 % (eine HIV-Infektion bei 1100 Expositionen). In allen Fällen werden auch hier individuelle Unterschiede durch die infektiöse Blutmenge, die Viruskonzentration und die Expositionsdauer bestimmt.
Risiko für eine HIV-Übertragung nach Art der Exposition dargestellt im Verhältnis zum Durchschnitt

Indikation zur HIV-PEP bei beruflicher Exposition
Eine HIV-PEP sollte bei Kontakten mit erhöhtem Infektionsrisiko empfohlen werden. Als solche gelten die perkutane Stichverletzung mit Injektionsnadel oder anderer Hohlraumnadel und die Schnittverletzung unter Beteiligung von Körperflüssigkeiten mit potentiell hoher HIVKonzentration.
Eine HIV-PEP kann angeboten werden bei Schleimhautkontakt oder Kontakt mit nicht-intakter Haut (Hautekzem, frischer Wunde etc.) mit Flüssigkeiten von hoher Viruskonzentration oder bei sichtbaren Verletzungen z. B. mit einer blutig-tingierten chirurgischen Nadel.
Eine HIV-PEP ist nicht indiziert bei allen fraglichen HIV-Expositionen ohne bzw. mit geringem Risiko. Dies betrifft etwa den perkutanen Kontakt zu Flüssigkeiten niedrigen Risikos wie Urin oder Speichel oder den Kontakt von infektiösem Material jeden Risikos zu intakter Haut
HIV-positive medizinische Beschäftigte und die Indikation zur HIV-PEP für exponierte Patienten
Nach jeder Exposition eines Patienten durch Blut eines HIV-positiven medizinischen Beschäftigten oder dem begründeten Verdacht darauf, ist (bei HIV-Positiven unter der Nachweisgrenze bei „massiver Inokulation von Blut“ bzw. bei HIV-Positiven mit nachweisbarer Viruslast ) ggf. bis zur genaueren Risikobewertung soweit möglich unmittelbar - auch in Narkose - eine HIV-PEP einzuleiten. Entsprechende fachliche und organisatorische Maßnahmen sollten in Einrichtungen von HIV-medizinischem Personal bereits im Vorfeld getroffen werden. Detaillierte Informationen siehe Leitlinie
Indikation zur HIV-PEP bei beruflicher HIV-Exposition (Indexperson HIV-positiv)
Standardprophylaxe
Aus pragmatischen Überlegungen werden an dieser Stelle nicht alle in Betracht kommenden Kombinationen aufgezählt und bewertet. Bewusst wird eine Kombination als Standard-PEP empfohlen, wobei durchaus alternativ auch andere Medikamente zum Einsatz kommen können.
Empfehlung zu PEP-Medikamenten

Veränderungen der Standard-PEP sind möglich, sollten aber durch in der HIV-Behandlung erfahrene Ärzt_innen vorgenommen werden. Die Prophylaxe sollte über 28-30 Tage durchgeführt werden. Längere Behandlungszeiträume können in Erwägung gezogen werden, wenn es zu einer massiven Kontamination gekommen ist und/oder der Zeitraum zwischen Exposition und Prophylaxebeginn länger als 36-48 Stunden ist (Expertenkonsultation!).
Unerwünschte Wirkungen
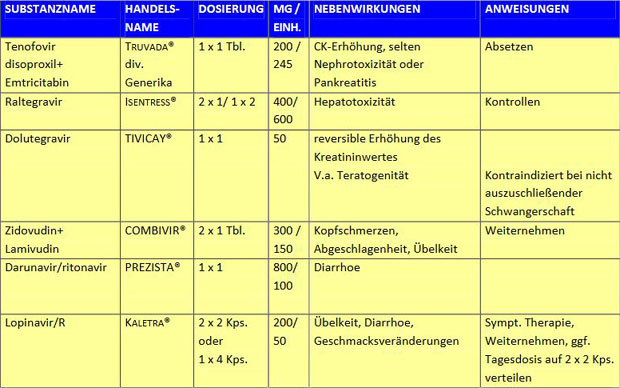
Die Nebenwirkungen der antiretroviralen Medikamente sind bei gesunden Menschen und bei kurzer Therapiedauer gering und reversibel (siehe hierzu Tabelle). Gastrointestinale Beschwerden, Abgeschlagenheit und Kopfschmerzen gehören zu den häufigsten unerwünschten Wirkungen. Unter der Therapie mit Nukleosidanaloga wurden verschiedentlich metabolische Syndrome bis zur Laktatazidose und Pankreatitiden beschrieben, die jedoch bei kurzfristiger prophylaktischerGabe ebenfalls kaum zu erwarten sind. Dennoch bedürfen vor allem Personen mit prädisponierenden Faktoren wie eingeschränkter Leberfunktion diesbezüglich einer besonderen ärztlichen Überwachung.
Dosierung und wesentliche unerwünschte Wirkung (auch bei Schwangerschaft) von antiretroviralen Medikamenten, die für eine PEP empfohlen wurden
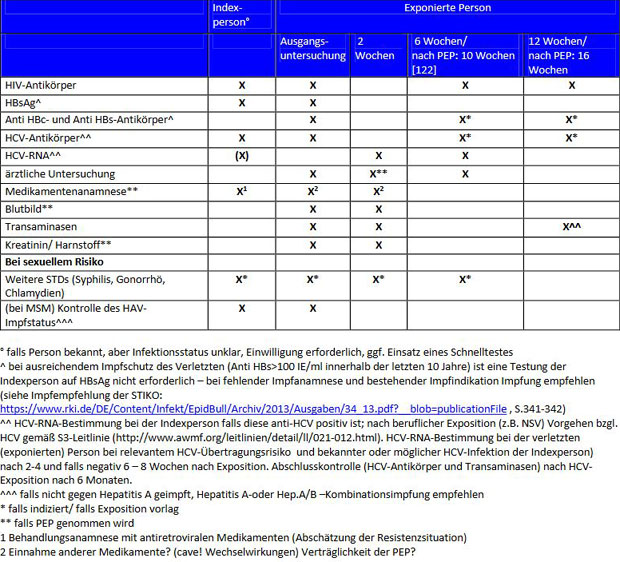
Laborkontrollen
Experten-Konsultation
Die langjährige Erfahrung mit postexpositioneller Prophylaxe einer HIV-Infektion im medizinischen Bereich zeigt, dass trotz ausführlicher nationaler und internationaler Leitlinien individuelle Besonderheiten der HIV-Exposition immer wieder den Rat von im Umgang mit der PEP erfahrenen Experten erfordern. Ein solcher Rat von in der HIV-Therapie erfahrenen Ärztinnen und Ärzten sollte in der Regel zeitnah nach Einleitung jeder PEP eingeholt werden, insbesondere aber dann, wenn die Indikation sowie die Art und der Umfang der Prophylaxe im Rahmen dieser Empfehlungen nicht eindeutig geregelt sind.
Sofern vor Ort kein Rat von ausgewiesenen Experten eingeholt werden kann oder diese nichtbekannt sind, kann hierfür auch - allerdings nur während der üblichen Arbeitszeiten (Mo.-Fr. ca. 9.00 - 17.00) das RKI (Tel: 030/18754 3467) in Anspruch genommen werden, über das auch eine Vermittlung an Experten in der Nähe erfolgen kann. Ausserhalb der Dienstzeiten kann über die Infektionsepidemiologische Rufbereitschaft Rat eingeholt werden (Tel: 030/18754-0).
Eine ad-hoc Telefonberatung für Notsituationen (Screening- und ggf. Verweis-Funktion an mögliche Behandler, nicht jedoch Indikationsstellung und/oder medizinische Interventionsberatung) bietet auch die Bundeszentrale für gesundheitliche Aufklärung (BZgA) mit Beratungszeiten täglich ab 10 Uhr, Mo-Do bis 22 Uhr, Fr-So bis 18 Uhr (Tel: 0221/ 892031).
Die Deutsche AIDS-Hilfe bietet auf der Homepage des HIVReport (www.hivreport.de) eine Liste der Kliniken, die 24 Stunden am Tag eine Beratung zur HIV-PEP durchführen können (Selbstauskunft der Kliniken und Testanrufe).
Auf der Homepage der österreichischen AIDS-Gesellschaft (www.aidsgesellschaft.info) findet sich ebenfalls eine Liste der österreichischen HIV-Behandlungszentren, die bei Fragen zur HIV-PEP kontaktiert werden können.
Kostenübernahme
Alle genannten Arzneimittel sind für die HIV-PEP nicht zugelassen. Kostenerstattung erfolgt über die
Berufsgenossenschaft.
* Die deutsch-österreichischen Empfehlungen zur PEP wurden im Sommer 2018 aktualisiert und sind in voller Länge
auf der Homepage www.daignet.de einzusehen.










 Diese Seite weiter empfehlen
Diese Seite weiter empfehlen
