Ulrich Seybold, München
Update Impfungen bei Menschen mit HIV-Infektion
Die Ständige Impfkommission (STIKO) am Robert Koch-Institut empfiehlt, jeden Arztbesuch zu nutzen, um die Impfdokumentation zu überprüfen und den Impfschutz zu vervollständigen.1 Der regelmäßige und langjährige Kontakt im Rahmen der Betreuung von PLHA bietet durch das im Rahmen anderer Arzt-Patient-Beziehungen oft nicht erreichbare Vertrauensverhältnis die einzigartige Möglichkeit, das inzwischen in Teilen der Gesellschaft hochemotional und häufig irrational diskutierte Thema Impfen faktenbasiert und auf die jeweilige Situation spezifisch angepasst zu besprechen.
Inzwischen wurden von einer STIKO-initiierten Expertengruppe spezifische Empfehlungen auch für die Impfung von PLHA publiziert.2 Diese weichen allerdings z.T. von den allgemeinen STIKO-Empfehlungen ab, in diesen Fällen sollte daher ggfs. die Kostenübernahme durch die Krankenkasse im Vorfeld überprüft werden.

Nur der Impfpass ist verlässlich
Der aktuelle Impfstatus sollte bereits im Rahmen der Erstvorstellung erhoben werden.3,4 Erinnerungen an durchgemachte Erkrankungen bzw. erfolgte Impfungen sind generell unsicher, daher sollen nur dokumentierte Impfdosen vorausgesetzt werden. Somit ist die Suche nach dem Impfpass bzw. seine Rekonstruktion anhand verfügbarer Dokumentation der erste notwendige Schritt. Besteht Unklarheit bzgl. des Impfstatus, sollte eine Grundimmunisierung gemäß den Empfehlungen für Nachholimpfungen erfolgen.
Bei ausgeprägtem Immundefekt (CD4+-Helferzellen (CD4) <200/µl) sind Lebendimpfungen generell kontraindiziert, andere Impfungen können weniger effektiv sein. Gleichzeitig ist aber die Gefährdung durch Infektionen höher. Indizierte Impfungen sollten daher generell nicht aufgeschoben werden, eine Wiederholung nach erfolgter Immunrekonstitution kann in vielen Fällen sinnvoll sein.2-4 Für einige Infektionserkrankungen sind Antikörper-Titer definiert, über denen ein ausreichender Schutz angenommen wird. So kann die Notwendigkeit einiger möglicherweise kontraindizierter, aufwändiger, derzeit wenig erfolgversprechender oder sonst problematischer Impfungen überprüft werden (Tab. 1).
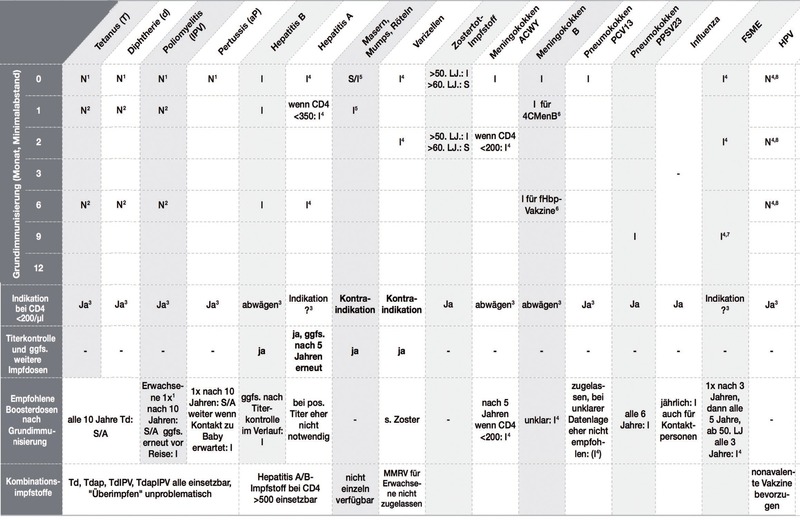
I: Medizinische/epidemiologische Indikation, N: Nachholimpfung, A: Auffrischimpfung, S: Standardimpfung, R: Reiseimpfung
1) zweckmäßig mit Tdap-IPV 4-fach-Impfstoff
2) zweckmäßig mit Td-IPV 3-fach-Impfstoff
3) ggfs. Wiederholung nach Immunrekonstitution
4) gem. STIKO keine Indikation durch HIV-Infektion: sonstige Indikation oder ggfs. Kostenübernahme prüfen!
5) STIKO-Empfehlung abweichend: Masern 1x (S), Röteln bei ♀ 2x (I) (Mumps 1x nur bei beruflicher Indikation)
6) Mindestabstand für 4CMenB (Bexsero®) 1 Monat, für fHbp-Vakzine (Trumenba®) 6 Monate
7) je nach Präparat 5-12 (FSME-Immun®) oder 9-12 (Encepur®) Monate nach der 2. Dosis
8) optimal 9-fach Vakzine; STIKO-Empfehlung nur für < vollendetes 18. LJ. EACS-Empfehlung bis 26. LJ, bei MSM bis 40. LJ
Tab. 1 Für PLHA empfohlene Impfungen mit STIKO-Indikationskategorie bei nicht ausreichender/nicht ausreichend dokumentierter Immunisierung nach1-3
Tetanus/Diphtherie/Pertussis
Trotz rückläufigen Trends erhalten in Deutschland 95% der Kinder 4 Dosen der Tetanus-/ Diphtherie-/ Pertussis-Vakzine (T-d-ap)5 und 94% 3 Dosen Polio-Vakzine (IPV).6 Trotzdem hat die Inzidenz von Pertussis von 116 Fällen im Jahr 2001 auf seit 2016 >20.000 Fälle pro Jahr zugenommen.7 Grund hierfür ist wohl v.a. ein schnellerer Abfall der protektiven Immunität des seit den 1990er Jahren verwendeten azellulären Impfstoffs.
Mit oder ohne Polio?
Trotz der beinahe-Eradikation von Poliomyelitis traten 2018 in Pakistan und Afghanistan weiterhin Wildtyp-Polio-Erkrankungsfälle auf und auch die Liste der Länder mit Ausbrüchen durch zirkulierende Vakzine-abgeleitete Polioviren ist mit der DR Kongo, Niger, Nigeria, Somalia und zuletzt auch Papua-Neuguinea wieder länger geworden. Zu den Risikoländern zählt neben Syrien und Irak u.a. auch das EU-Nachbarland Ukraine. Aufgrund eines Versorgungsengpasses mit inaktiviertem Polioimpfstoff ist es zudem in einigen Entwicklungs- und Schwellenländern zu signifikanten Polioimpflücken gekommen8, was die Gefahr großräumiger Ausbrüche sehr real macht. Damit sind Daten aus Nachbarländern sowohl nachvollziehbar als auch alarmierend: In einer repräsentativen Kohorte von PLHA aus Österreich war nur bei 1% ein Schutz gegen Pertussis und auch nur bei 51% gegen Tetanus nachweisbar.9 Bei PLHA mit afrikanischen Wurzeln in Frankreich hatten lediglich ca. je 70% protektive Antikörpertiter gegen Tetanus und Diphtherie und weniger als 65% gegen Polio.10 Gefährdet waren vor allem Migranten, insgesamt hatten 95% der PLHA mit CD4-Werten >200/µl insuffiziente Titer für mindestens eine der Tdap-Komponenten.9
Erneute Grundimmunisierung
Bei
nicht ausreichend dokumentiertem Impfstatus muss eine (ggfs. erneute)
Grundimmunisierung durchgeführt werden. Die STIKO hat klargestellt,
dass bei Erwachsenen dafür die in Deutschland verfügbaren 4- und
3-fach-Impfstoffe verwendet werden sollen1:
nach einer Dosis Tdap-IPV folgen 1 und 6 Monate später weitere Dosen
Td-IPV. Td sollte regelmäßig alle 10 Jahre aufgefrischt, die
nächste Boosterdosis als Tdap gegeben werden. Bei Tätigkeit im
Gesundheitswesen sowie erwartetem engen Kontakt zu Neugeborenen
sollten alle 10 Jahre weitere ap-Auffrischungen erfolgen. Auch für
IPV ist ein Booster im Erwachsenenalter indiziert, sollte dieser
länger als 10 Jahre zurückliegen, so ist bei entsprechenden
Reiseplänen eine weitere Auffrischung angezeigt, die dann als
Kategorie „I“-Impfung im Gegensatz zu sonstigen
Reiseimpfungen durch die Krankenkassen übernommen werden muss. Eine
evtl. unnötig häufige Impfung ist nicht gefährlich, bei sehr engem
Abstand von <4 Wochen kann aber mit einer erhöhten Inzidenz von
schmerzhaften Lokalreaktionen gerechnet werden.
Hepatitis B
Die Hepatitis-B-Impfung ist für alle HBV-naiven PLHA indiziert1-4,11,12 und erfolgt als dreimalige Gabe (0, 1, 6 Monate), insbesondere bei CD4 <500/µl bevorzugt mit einem Einzelimpfstoff. Eine Titerkontrolle sollte mindestens 4 Wochen nach der dritten Dosis erfolgen, um ein ausreichendes Ansprechen zu dokumentieren. Dieses ist wahrscheinlicher bei gutem Immunstatus und supprimierter HI-Viruslast, zur Steigerung des Impferfolgs kann die Kombination mit anderen Impfstoffen (z.B. adjuvantierte Td-haltige Vakzine13) erwogen werden. Im Falle einer Non-Response (anti-HBs <10 IU/l) oder einer Low Response (anti-HBs <100 IU/l) werden zuerst weitere Dosen gegeben. Bei anhaltend zu niedrigem anti-HBs-Titer und dringender Indikation kann der (allerdings nur bei Niereninsuffizienz zugelassene) adjuvantierte HBV-Impfstoff erwogen werden.2,4 Der nicht adjuvantierte aber höher dosierte Impfstoff ist nur bei schwerer Niereninsuffizienz (Prädialyse, Dialyse) zugelassen und noch teurer. Eine weitere (aber generell nicht zugelassene!) Möglichkeit zur Überwindung einer Non-Response ist die intrakutane Applikation der „normalen“ Vakzine, allerdings können hier starke Lokalreaktionen und z.T. bleibende Discolorationen auftreten. Über diese möglichen Nebenwirkungen und den off-label-Gebrauch muss daher unbedingt aufgeklärt werden. Die Erfahrung in unserer Ambulanz zeigt, dass durch die (mehrfach) wiederholte ggfs. intracutane Gabe bei den meisten PLHA ein protektiver anti-HBs-Titer erreicht werden kann.
Hepatitis A
Die STIKO1 definiert ebenso wie die meisten anderen relevanten Expertengruppen2-4,12 weiterhin eine HIV-Infektion nicht als Grund für eine Hepatitis-A-Impfung, allerdings ist diese bei vielen PLHA durch andere Umstände indiziert, wie etwa eine Lebererkrankung, häufige Übertragung von Blutbestandteilen (z.B. bei Hämophilie oder Drogenkonsum) und bei „Sexualverhalten mit erhöhtem Expositionsrisiko“.1 Aufgrund gelegentlicher Ausbrüche kann die HAV-Impfung aber auch generell für PLHA erwogen werden.11 Als freiwillige Satzungsleistung werden die Kosten inzwischen von vielen Kassen ohnehin übernommen. Aufgrund der bei PLHA selteneren Serokonversion bei Verwendung des üblichen 2-Dosenschemas oder des bzgl. der HAV-Komponente niedriger dosierten HAV/HBV-Kombinationsvakzine sind bei CD4 <350/µl 3 Dosen und bei <500/µl 2 Dosen eines Einzelimpfstoffs empfohlen, der Kombinationsimpfstoff sollte allenfalls bei PLHA mit CD4 >500/µl erwogen werden. Eine Titerkontrolle nach der Grundimmunisierung ist sinnvoll. Bei möglicherweise auch reduzierter Durabilität der Protektion sollte alle 5 Jahre der Titer kontrolliert werden2, andere Experten empfehlen auch 10-jährliche Routine-Boosterdosen.4
Masern, Mumps, Röteln und Windpocken
Über 90% der deutschen Kinder sind gegen Masern/Mumps/Röteln (MMR) geimpft, trotzdem zeigten sich in einer Querschnittsuntersuchung bei erwachsenen PLHA nicht sicher protektive Titer bei 8% für Masern, 26% für Mumps, 10% für Röteln und 3% für VZV.14 Masernausbrüche treten auch in Deutschland immer wieder auf, die jährlichen Meldezahlen lagen in den letzten Jahren zwischen wenigen Hundert und einigen Tausend. In vielen Ländern ist derzeit aufgrund ungenügender Impfquoten ein dramatischer Anstieg von Masernfällen zu verzeichnen. Dieser Trend hat Deutschland bisher nicht erreicht, aber auch hier treten Impfgegner immer aggressiver auf. Bei PLHA verlaufen insbesondere Masern und Varizellen häufig kompliziert, die Diagnose kann durch atypische Verläufe verzögert sein. Bei MMR-1-4,11,12 oder VZV-2-4,11,12 seronegativen PLHA ist daher die jeweilige Impfung indiziert.
MMR-Impfung
Nach
Masernimpfungen wurden bei ausgeprägtem Immundefekt Fälle mit
schweren und teilweise tödlichen Komplikationen beschrieben.4,15
Daher dürfen Lebendimpfstoffe ausschließlich bei stabilem
Immunstatus mit CD4 >200/µl/ >14% der Lymphozyten verwendet
werden. Im Unterschied zur STIKO empfehlen Experten für die
MMR-
Impfung von PLHA die Verwendung von 2 Dosen im Abstand von >1
Monat. Die von der STIKO nicht aufgrund von HIV indiziert gesehene
VZV-Impfung erfolgt bei PLHA mit 2 Dosen im Abstand von 12 Wochen.2,4
Eine Titerkontrolle und ggfs. weitere Impfdosen sind jeweils
sinnvoll. Mehrere Lebendimpfstoffe sollen generell entweder
gleichzeitig oder im Abstand von >1 Monat appliziert werden.
Herpes Zoster
Seit 2018 ist ein rekombinanter, adjuvantierter Untereinheiten-Totimpfstoff zur Prävention von Herpes Zoster und Post-Zoster-Neuralgie verfügbar, der in den Zulassungsstudien eine Vakzineffektivität von >90% bzgl. Schutz vor Zoster und bis zu 100% bzgl. Neuralgie zeigte.16,17 Untersuchungen zur Immunogenität bei PLHA waren ermutigend.18 In allen Studien zeigte sich aber eine ausgeprägte Reaktogenität mit Grad 3 Lokalreaktionen bei 8,5-16% der Geimpften. Daher sollte auch die subcutane Gabe unbedingt vermieden werden. Die Zulassung besteht für PLHA und Menschen mit anderen Immundefekten ab 50 Jahren, für Immungesunde ab 60 Jahren. Die Impfung erfolgt mit 2 Dosen zu den Zeitpunkten 0 und 2 (-6) Monaten. Die Kostenübernahme ist nach Publikation des G-BA-Beschlusses zur Aufnahme dieser Impfung in die Schutzimpfungsrichtlinie für die gesetzlichen Krankenversicherungen seit 01.05.2019 verpflichtend. Bei einer Lebenszeitprävalenz von 20-30% bereits in der Allgemeinbevölkerung19 ist diese Impfung für PLHA klar indiziert.1,2
Die Indikation gilt insbesondere auch für Menschen, die sich nicht an durchgemachte Windpocken erinnern, die bereits Zoster hatten, die schon den „alten“ Lebendimpfstoff erhalten haben, bei denen andere chronische Erkrankungen oder ein ausgeprägter Immundefekt vorliegen oder die ein fortgeschrittenes Lebensalter erreicht haben.20 Eine weitere Boosterdosis nach der Grundimmunisierung wird nicht empfohlen. Aufgrund fehlender Daten ist die Kombination bisher ausschließlich mit der Influenzaimpfung empfohlen.
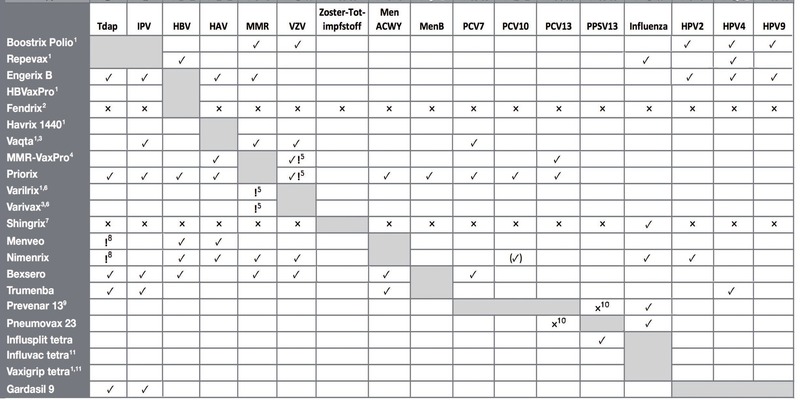
Legende:
✓: gleichzeitige Gabe bei Erwachsenen in Studien untersucht und unproblematisch
Zelle leer: gleichzeitige Gabe grundsätzlich möglich, aber nicht spezifisch untersucht
x: gleichzeitige Gabe nicht empfohlen
!: Besonderheiten bei der sequenziellen Gabe
Impfstoffe:
T: Tetanus,
d:
Diphterie, ap:
Pertussis,
IPV: Poliomyelitis,
HBV:
Hepatitis B,
HAV:
Hepatitis A,
MMR:
Masern/Mumps/Röteln,
VZV:
Windpocken,
Men:
Meningokokken,
PCV:
Pneumokokken-Konjugatvakzine,
PPSV:
Pneumokokken-Polysaccharid-Vakzine, Influenza:
nicht
adjuvantierter Totimpfstoff, HPV:
Humanes Papillomvirus
1) die Kombination mit anderen Impfstoffen wird als generell unproblematisch angegeben
2) aufgrund unzureichender Datenlage ist keine Kombination mit anderen Impfungen empfohlen, 2-3 Wochen Mindestabstand
3) nur Studiendaten zu Kindern verfügbar
4) Analogieschluss aufgrund von Studiendaten zu anderen Präparaten
5) Lebendimpfungen entweder gleichzeitig oder mind. 1 Monat Abstand
6) keine Anwendung von ASS im Zeitraum von 6 Wochen nach einer VZV-Lebendimpfung
7) aufgrund fehlender Studiendaten nur Kombination mit Influenzaimpfstoff empfohlen
8) gleichzeitig oder MenACWY >1 Monat vor Tdap
9) keine Studiendaten zur Kombination mit anderen Impfstoffen bei 18-49-Jährigen
10) optimale Sequenz: zuerst PCV13, nach 6-12 Monaten PPSV23
11) keine Studiendaten zu Wechselwirkungen
Tab. 2 Angaben der Fachinformation (linke Spalte) zu Wechselwirkungen von ausgewählten Impfstoffen
Meningokokken
In Deutschland waren invasive Meningokokkenerkrankungen (IMD) in den letzten Jahren mit ca. 300-350 Fällen pro Jahr selten. Hauptsächlich betroffen sind Kinder, kleinere Altersgipfel bestehen bei Jugendlichen und jungen Erwachsenen sowie Menschen im hohen Alter.21 Allerdings kommt es immer wieder zu Clustern, wie etwa 2012/13 in Berlin.22 Bei PLHA besteht ein mit 5-24-fach mäßig erhöhtes Risiko für IMD.23,24
In
Deutschland ist die Verwendung von Meningokokken-Konjugatimpfstoffen
bei Immundefekt allgemein empfohlen1,
die auch von anderen Experten2,
3,11,12,24,25 gesehene
Indikation für PLHA ist also bzgl. der Kostenübernahme generell
abgesichert. Allerdings sollte im Unterschied zu Immungesunden
für die Grundimmunisierung gegen 4 Serogruppen (MenACWY) zumindest
bei ausgeprägtem Immundefekt (CD4 <200/µl) nach frühestens 8
Wochen eine 2. Dosis gegeben werden, außerdem nach 5 Jahren eine
Boosterdosis.2
Andere Experten empfehlen dieses Vorgehen generell für PLHA.3,4,24
Die
Grundimmunisierung gegen die in Deutschland häufigste Serogruppe B
erfolgt grundsätzlich mit 2 Dosen. Hier muss für die beiden
verfügbaren Präparate der unterschiedliche Mindestabstand
berücksichtigt werden: für den 4-Komponentenimpfstoff (4CMenB)
beträgt er 1 Monat, für die Faktor H-bindende Protein-Vakzine
(fHbp) 6 Monate. Aufgrund nicht ausreichender Sicherheitsdaten und
einer vergleichsweise hohen Rate auch systemischer
Nebenwirkungen
soll die MenB-Impfung während einer Schwangerschaft nur bei
dringender, konkreter Indikation erfolgen.25
Zur Reduktion auch der nicht selten stärkeren Lokalreaktionen kann prophylaktisch Paracetamol gegeben werden, das die Antikörperantwort nicht beeinträchtigt.
Interessant
ist die Beobachtung eines moderaten protektiven Effekts einer
Meningokokken-B-Impfung gegen
Gonorrhoe26,27,
der bei Verwendung des in Deutschland verfügbaren 4CMenB-Impfstoffs
möglicherweise noch stärker ist.28
Damit muss die Indikation für die Impfung gegen die einerseits
seltene, andererseits aber mit einer Letalität von 5-10%21
auch gefährliche Meningokokken-Erkrankung unter Berücksichtigung
der individuellen Situation abgewogen werden.
Pneumokokken
Die Inzidenz von invasiven Pneumokokkenerkrankungen und der Pneumokokkenpneumonie ist bei PLHA deutlich erhöht.4 Gemäß der aktuellen STIKO-Empfehlung sollen PLHA zuerst den 13-valenten Konjugatimpfstoff (PCV13) und im Abstand von (6-) 12 Monaten den 23-valenten Polysaccharidimpfstoff (PPSV23) erhalten. Bei bereits dokumentierter PPSV23-Gabe sollte nach frühestens einem Jahr PCV13 verabreicht werden.1 Da das Risiko für Pneumokokkenerkrankungen mit dem Ausmaß des Immundefekts zunimmt, das Impfansprechen für PCV13 und PPSV23 aber auch bei niedrigen CD4+-Helferzellen nicht beeinträchtigt ist2, sollte die Impfung sofort nach HIV-Diagnose erfolgen.2-4,12 Die Indikation für die nach STIKO empfohlene Booster-Dosis PPVS23 alle 6 Jahre1,2 wird international nicht einheitlich gesehen.4,11 Aufgrund der besseren Immunogenität wäre auch die (bei PLHA zugelassene) Boosterung mit PCV13 möglich29,30, allerdings ist hier für eine konkrete Empfehlung die Datenbasis unzureichend.
Influenza
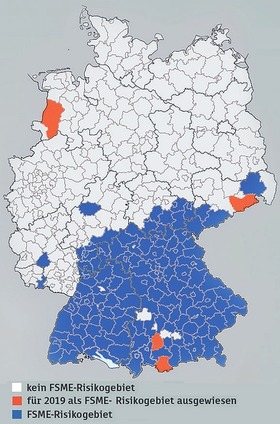
FSME-Risikogebiete in Deutschland
©Robert Koch-Institut, Foto: dpa
In Deutschland wurden 2017/18 ca. 45.000 Personen aufgrund von Influenza hospitalisiert, mindestens 25.000 starben an Influenza. 38% der gemeldeten Fälle traten bei Menschen zwischen 35 und 49 Jahren auf.31 Besonders gefährdet sind insbesondere PLHA.32 Daher ist die jährliche Influenza-Impfung für alle PLHA eindeutig empfohlen.1-4,11,12,32 Nicht vernachlässigt werden sollte die ebenfalls indizierte Impfung von Personen z.B. im selben Haushalt, die PLHA als Infektionsquelle gefährden könnten, da die ohnehin nur mäßige Vakzineffektivität durch Immundefekte zusätzlich eingeschränkt ist. Die Zahl der verfügbaren saisonalen Totimpfstoffe ist seit der ausschließlichen Empfehlung quadrivalenter Vakzine33 deutlich zurückgegangen, belegbare Unterschiede bzgl. Wirksamkeit oder Verträglichkeit bestehen nicht.
FSME
Die Indikation für die FSME-Impfung unterscheidet sich bei PLHA nicht von der Allgemeinbevölkerung, betrifft also alle Menschen, die in FSME-Risikogebieten Zecken exponiert sind.1 Die Zahl der FSME-Fälle in Deutschland nimmt in den letzten Jahren eher zu, inzwischen sind neben Gebieten in Rheinland-Pfalz, Hessen, Thüringen, Sachsen und erstmals Nordrhein-Westfalen praktisch alle Kreise in Baden-Württemberg und Bayern Risikogebiete. Ausnahmen sind hier lediglich der Stadtkreis Heilbronn, die Landkreise Dillingen an der Donau und Fürstenfeldbruck sowie die Stadtkreise Augsburg, München und Schweinfurt.34 Für diese statistisch nicht als Risikogebiete definierten Stadtkreise muss aber berücksichtigt werden, dass bei entsprechender Zeckenexposition trotzdem FSME übertragen werden kann, eine Impfung also möglicherweise sinnvoll ist. Nicht unterschätzt werden sollte außerdem die FSME-Gefahr bei Reisen insbesondere in die Schweiz, nach Österreich, Osteuropa und in baltische Länder.35
1 Robert Koch-Institut. Empfehlungen der Ständigen Impfkommission (STIKO) am Robert Koch-Institut - 2018/2019. Epid Bull 2018;34:335-382
2 Ehl S, Bogdan C, Niehues T, et al. Impfen bei Immundefizienz: Anwendungshinweise zu den von der Ständigen Impfkommission empfohlenen Impfungen. (II) Impfen bei 1. Primären Immundefekterkrankungen und 2. HIV-Infektion. Bundesgesundheitsblatt Gesundheitsforschung Gesundheitsschutz 2018;61:1034-1051
3 European AIDS Clinical Society. Guidelines - Version 9.1. Verfügbar unter http://www.eacsociety.org/files/2018_guidelines-9.1-english.pdf. 2018
4 British HIV Association. Guidelines on the use of vaccines in HIV-positive adults. Verfügbar unter http://www.bhiva.org/documents/Guidelines/Vaccination/2015-Vaccination-Guidelines.pdf. 2015
5 World Health Organization. Reported estimates of DTP4 coverage, Stand 18. September 2018. Verfügbar unter http://apps.who.int/immunization_monitoring/globalsummary/timeseries/tscoveragedtp4.html . Letzter Zugriff am 29.04.2019. 2018
6 World Health Organization. Third dose of polio vaccine, Stand 18. September 2018. Verfügbar unter http://apps.who.int/immunization_monitoring/globalsummary/timeseries/tscoveragepol3.html . Letzter Zugriff am 29.04.2019. 2018
7 Robert Koch-Institut. SurvStat@RKI 2.0. Web-basierte Abfrage der Meldedaten gemäß Infektionsschutzgesetz (IfSG). 2019; verfügbar unter https://survstat.rki.de/Content/Query/Create.aspx . Abfrage am 26. März 2019
8 Sutter RW, Cochi SL. Inactivated Poliovirus Vaccine Supply Shortage: Is There Light at the End of the Tunnel? J Infect Dis 2019
9 Grabmeier-Pfistershammer K, Herkner H, Touzeau-Roemer V, Rieger A, Burgmann H and Poeppl W. Low tetanus, diphtheria and acellular pertussis (Tdap) vaccination coverage among HIV infected individuals in Austria. Vaccine 2015;33:3929-32
10 Mullaert J, Abgrall S, Lele N, et al. Diphtheria, tetanus, poliomyelitis, yellow fever and hepatitis B seroprevalence among HIV1-infected migrants. Results from the ANRS VIHVO vaccine sub-study. Vaccine 2015;33:4938-44
11 U.S. Department of Health and Human Services, Health Resources and Services Administration. Guide for HIV/AIDS Clinical Care – 2014 Edition. Rockville, MD: U.S. Department of Health and Human Services, 2014
12 Centers for Disease Control and Prevention. HIV Infection and Adult Vaccination. Verfügbar unter https://www.cdc.gov/vaccines/adults/rec-vac/health-conditions/hiv.html . Letzter Zugriff am 1. Mai 2019. 2016
13 Sonmez E, Sonmez AS, Bayindir Y, Coskun D and Ariturk S. Antihepatitis B response to hepatitis B vaccine administered simultaneously with tetanus toxoid in nonresponder individuals. Vaccine 2002;21:243-6
14 Schwarze-Zander C, Draenert R, Lehmann C, et al. Measles, mumps, rubella and VZV: importance of serological testing of vaccine-preventable diseases in young adults living with HIV in Germany. Epidemiol Infect 2017;145:236-244
15 Su JR, Ng C, Lewis PW and Cano MV. Adverse events after vaccination among HIV-positive persons, 1990-2016. PLoS One 2018;13:e0199229
16 Cunningham AL, Lal H, Kovac M, et al. Efficacy of the Herpes Zoster Subunit Vaccine in Adults 70 Years of Age or Older. N Engl J Med 2016;375:1019-32
17 Lal H, Cunningham AL, Godeaux O, et al. Efficacy of an adjuvanted herpes zoster subunit vaccine in older adults. N Engl J Med 2015;372:2087-96
18 Berkowitz EM, Moyle G, Stellbrink HJ, et al. Safety and immunogenicity of an adjuvanted herpes zoster subunit candidate vaccine in HIV-infected adults: a phase 1/2a randomized, placebo-controlled study. J Infect Dis 2015;211:1279-87
19 Ultsch B, Weidemann F, Koch J and Siedler A. Projektbericht - Modellierung von epidemiologischen und gesundheitsökonomischen Effekten von Impfungen zur Prävention von Herpes zoster. Verfügbar unter https://www.rki.de/DE/Content/Infekt/Impfen/ImpfungenAZ/Zoster/Modellierung_Zoster_Impfung.pdf. Robert Koch-Institut 2017
20 Dooling KL, Guo A, Patel M, et al. Recommendations of the Advisory Committee on Immunization Practices for Use of Herpes Zoster Vaccines. MMWR Morb Mortal Wkly Rep 2018;67:103-108
21 Robert
Koch-Institut. Infektionsepidemiologisches Jahrbuch meldepflichtiger
Krankheiten für 2017. 2018;Verfügbar unter
https://www.rki.de/DE/
Content/Infekt/Jahrbuch/Jahrbuch_2017.pdf.
Letzter Zugriff am 1. Mai 2019
22 Marcus U, Vogel U, Schubert A, et al. A cluster of invasive meningococcal disease in young men who have sex with men in Berlin, October 2012 to May 2013. Euro Surveill 2013;18
23 Miller L, Arakaki L, Ramautar A, et al. Elevated risk for invasive meningococcal disease among persons with HIV. Ann Intern Med 2014;160:30-7
24 MacNeil JR, Rubin LG, Patton M, Ortega-Sanchez IR and Martin SW. Recommendations for Use of Meningococcal Conjugate Vaccines in HIV-Infected Persons - Advisory Committee on Immunization Practices, 2016. MMWR Morb Mortal Wkly Rep 2016;65:1189-1194
25 Kim DK, Hunter P. Advisory Committee on Immunization Practices Recommended Immunization Schedule for Adults Aged 19 Years or Older - United States, 2019. MMWR Morb Mortal Wkly Rep 2019;68:115-118
26 Paynter J, Goodyear-Smith F, Morgan J, Saxton P, Black S and Petousis-Harris H. Effectiveness of a Group B Outer Membrane Vesicle Meningococcal Vaccine in Preventing Hospitalization from Gonorrhea in New Zealand: A Retrospective Cohort Study. Vaccines (Basel) 2019;7, E5
27 Petousis-Harris H, Paynter J, Morgan J, et al. Effectiveness of a group B outer membrane vesicle meningococcal vaccine against gonorrhoea in New Zealand: a retrospective case-control study. Lancet 2017;390:1603-1610
28 Semchenko EA, Tan A, Borrow R and Seib KL. The serogroup B meningococcal vaccine Bexsero elicits antibodies to Neisseria gonorrhoeae. Clin Infect Dis 2018, ePub ahead of Print
29 Frenck RW, Jr., Fiquet A, Gurtman A, et al. Immunogenicity and safety of a second administration of 13-valent pneumococcal conjugate vaccine 5 years after initial vaccination in adults 50 years and older. Vaccine 2016;34:3454-62
30 Jackson LA, Gurtman A, van Cleeff M, et al. Influence of initial vaccination with 13-valent pneumococcal conjugate vaccine or 23-valent pneumococcal polysaccharide vaccine on anti-pneumococcal responses following subsequent pneumococcal vaccination in adults 50 years and older. Vaccine 2013;31:3594-602
31 Robert Koch-Institut. Bericht zur Epidemiologie der Influenza in Deutschland Saison 2017/18. Verfügbar unter https://influenza.rki.de/Saisonberichte/2017.pdf. 2018
32 World Health Organization. Vaccines against influenza, WHO position paper – November 2012. Weekly epidemiological record 2012;87:461-476
33 Robert Koch-Institut. Mitteilung der Ständigen Impfkommission am Robert Koch-Institut: Wissenschaftliche Begründung für die Empfehlung des quadrivalenten saisonalen Influenzaimpfstoffs. Epid Bull 2018;2:19-31
34 Robert Koch-Institut. FSME: Risikogebiete in Deutschland (Stand: Januar 2019) - Bewertung des örtlichen Erkrankungsrisikos. Epid Bull 2019;7
35 Beaute J, Spiteri G, Warns-Petit E and Zeller H. Tick-borne encephalitis in Europe, 2012 to 2016. Euro Surveill 2018;23:pii=1800201











 Diese Seite weiter empfehlen
Diese Seite weiter empfehlen
