5 th IAS Conference on HIV Pathogenesis, Treatment and Prevention 19.-22. Juli 2009 in Kapstadt
Viel Politik, neue Therapiestrategien
Die 5. Tagung der Internationalen AIDS-Gesellschaft (IAS) fand im südafrikanischen Kapstadt statt. Wohl nicht zuletzt aus diesem Grund war Afrika ein wichtiges Thema auf der Konferenz – politisch und wissenschaftlich. Neben einigen interessanten Arbeiten aus USA und Europa gab es erstmals auch afrikanische Studien, deren Ergebnisse für alle anderen Länder der Welt relevant sind.
 Die internationale IAS-Tagung, die
jeweils in den Jahren zwischen den WeltAids-Konferenzen stattfindet, war
ursprünglich als „wissenschaftliche WeltAids-Konferenz“ angetreten. Dieses
Konzept wurde auf den ersten vier IAS-Tagungen auch konsequent umgesetzt. Auf
der 5. IAS-Tagung in Kapstadt war davon nicht mehr viel zu spüren. Die Politik
stand im Vordergrund. Gründe dafür waren zum einen sicherlich der Tagungsort im
südlichen Afrika, zum anderen möglicherweise ein Mangel an aufregenden neuen
Daten. In den Sitzungen wurden oft Themen der diesjährigen CROI rekapituliert
(z.B. HIV und Inflammation), bekannte Themen intensiviert (z.B. HAART als
Prävention) und zukünftige Optionen diskutiert (z.B. Roll-out der PrEP).
Dennoch gab es insbesondere in den Late Breaker Sessions einige sehr
interessante neue Arbeiten.
Die internationale IAS-Tagung, die
jeweils in den Jahren zwischen den WeltAids-Konferenzen stattfindet, war
ursprünglich als „wissenschaftliche WeltAids-Konferenz“ angetreten. Dieses
Konzept wurde auf den ersten vier IAS-Tagungen auch konsequent umgesetzt. Auf
der 5. IAS-Tagung in Kapstadt war davon nicht mehr viel zu spüren. Die Politik
stand im Vordergrund. Gründe dafür waren zum einen sicherlich der Tagungsort im
südlichen Afrika, zum anderen möglicherweise ein Mangel an aufregenden neuen
Daten. In den Sitzungen wurden oft Themen der diesjährigen CROI rekapituliert
(z.B. HIV und Inflammation), bekannte Themen intensiviert (z.B. HAART als
Prävention) und zukünftige Optionen diskutiert (z.B. Roll-out der PrEP).
Dennoch gab es insbesondere in den Late Breaker Sessions einige sehr
interessante neue Arbeiten.
HIV-Therapie verhindert Tuberkulose und Malaria
Im südlichen Afrika sind neben HIV insbesondere Tuberkulose und Malaria dringliche Probleme. Offenbar vermindert die HAART auch die Anfälligkeit für diese beiden Infektionskrankheiten. So betrug in einer Tagesklinik in Kapstadt, von der rund 15.000 Einwohner betreut werden, vor dem breiten Zugang zu HIV-Medikamenten im Jahr 2005 die HIV-Prävalenz 23% und die TB-Prävalenz (bei HIV-negativen und HIV-positiven Bewohnern) 3%. Eine erneute Erhebung nach Einführung der HAART im Jahr 2008, nachdem im untersuchten Stadtgebiet 31% der HIV-Infizierten antiretroviral behandelt wurden, zeigten einen signifikanten Rückgang der HIV- und TB-Prävalenz auf 25% bzw. TB-Prävalenz 1,8% (p=0,012). Hintergrund der Entwicklung ist nach Meinung der Autoren eine geringere Reaktivierungsrate der TB unter HAART oder eine geringere TB-Transmission durch einen höheren Anteil der diagnostizierten und behandelten TB-Koinfektionen (Middelkoop K et al. WELB105).
Eine abnehmende Malaria-Inzidenz unter HAART wurde in der großen afrikanischen DART-Studie beobachtet. Im ersten Jahr der Behandlung betrug die Inzidenz noch 591 pro 1.000 Personenjahre, im zweiten Jahr 476, im dritten Jahr 259 und bei mehr als drei Jahren Therapie 153 pro 1.000 Personenjahre. Zudem korrelierten jüngeres Alter, niedrige CD4-Zellzahl und niedriges Bildungsniveau signifikant mit der Malaria-Infektion. Die Autoren schlugen daher vor, insbesondere HIV-Patienten mit schlechtem Immunstatus und niedrigen Bildungsstand zusätzlich eine Cotrimoxazol-Prophylaxe zu geben. In Hochprävalenzgebieten vermindert Cotrimoxazol das Malaria-Risiko bei HIV-Patienten um 75%, zusätzlich zu einer HAART sogar um 92% (Barnes K MOSY503; Kasirye R et al. TUPDB104).
Malaria Erreger
Eröffnung im Zeichen der Finanzkrise
Die Eröffnung der 5. IAS-Konferenz in Kapstadt war geprägt von der Sorge um die finanziellen Ressourcen zur Bekämpfung von HIV/Aids. Mittlerweile werden zwar über vier Millionen Menschen in LMIC (Low and middle income countries) behandelt, doch noch immer haben sechs Millionen keinen Zugang zur lebensrettenden Therapie. Die Behandlung dieser Menschen plus der zunehmende Bedarf an Zweitlinientherapien werden in den kommenden Jahren zu einem drastischen Anstieg bei den notwendigen Ressourcen führen. Viyuseka Dabula, Generalsekretärin der Treatment Action Campain betonte, dass ohne eine weitere Steigerung der Investitionen bereits im Jahr 2012 90% der aktuellen Ressourcen für die Zweitlinientherapie verbraucht werden.
Dem gegenüber stehen die weltweite Finanzkrise, Ermüdungserscheinungen bei den privaten Spendern und neue medizinische Prioritäten auf der Agenda der öffentlichen Geldgeber. Die G8-Länder haben bei ihrem letzten Treffen HIV/Aids aus der Prioritätenliste gestrichen und ihre Verpflichtung zum weltweiten Zugang zur Therapie bis 2011 nicht erneuert, geschweige denn ihre alten Zusagen erfüllt.
HAART als Prävention
„Test and Treat“ lautet der Slogan der Befürworter der HAART als Prävention. „Erfinder“ und herausragender Aktivist dafür ist Julio Montaner, Vancouver, der das Konzept im Rahmen drohender Kürzungen für die antiretrovirale Therapie in Kanada entwarf und im heimatlichen British Columbia bereits durchgesetzt hat. Weiterentwickelt wurde es von Ruben Granich, WHO, der sein globales mathematisches Modell erneut auf der Konferenz vorstellte. Laut Granich würde die Behandlung aller HIV-Infizierter weltweit die HIV-Inzidenz innerhalb von 10 Jahren von 2% auf 0,1% vermindern und die Prävalenz bis 2050 um 95%.
Das Konzept ist allerdings nicht unwidersprochen. In einer amerikanischen Arbeit wurde berechnet, dass selbst bei einer jährlichen Testung aller Erwachsenen plus sofortiger Therapie der Anteil der HIV-Patienten mit einer Viruslast >500 Kopien/ml in Washington DC um lediglich 60% sinken würde (Walensky RP et al. LBPEC04). Zudem kritisieren Patientenorganisationen die Vernachlässigung von Menschenrechten zugunsten von öffentlicher Gesundheit (vergleiche Streiflicht S. 63). Aktuell ist die HAART als Prävention noch nicht offizielle WHO-Politik, doch im November wolle man darüber nachdenken, welche Evidenz notwendig wäre, meinte Teguest Guerma von der WHO-Abteilung HIV/AIDS (Montaner M SUSAT0501; Granich R MOPL101; Guerma T. SUSAT0505; Kippax S MOSS201; Akugizibwe P MOSS203).
PrEP und PEP
Zur Wirksamkeit der PrEP (Prä-Expositionsprophylaxe) gab es keine neuen Ergebnisse, dennoch wurde auch auf dieser Konferenz in einem eigenen Symposium darüber diskutiert, wie die PrEP breit eingesetzt werden könnte. Im Hinblick auf die PEP (Post-Expositionsprophylaxe) waren TDF/FTC/LPV/r bzw. TDF/FTC/RAL in einer französischen bzw. amerikanischen Studie deutlich verträglicher als der Standard AZT/3TC/PI/r (Tosini W et al. WEAC102; Mayer K et al. WEAC104).
Mikrobizide und Aciclovir
Bei den Mikrobiziden hatte Maraviroc die Experten enttäuscht. In Gewebekulturen von Vorhaut und Rektalschleimhaut verminderte der CCR5-Antagonist trotz hoher Konzentrationen die HIV-Transmission lediglich um 50-60% bzw. 85% (Fletcher PS et al. WEPDC201; Young K et al. WEPDC201). Die Gabe von Aciclovir (2x 400 mg/d) konnte in der „Partners in Prevention Study“ (n=3.408, zwei Drittel Frauen) die Wahrscheinlichkeit einer HIV-Übertragung auf den HIV-negativen Partner nicht vermindern, wohl aber die HIV-Progression. Das Risiko von Aids wurde im Lauf der zweijährigen HSV-2-Therapie um 17%, die Notwendigkeit einer HAART signifikant um 19% gesenkt (Celum C et al. WELBC101; Lingappa JR et al. WELBC102).
Keine Transmission durch Stillen
Bei der Mutter-Kind-Transmission gab es eine kleine Sensation. Erstmals wurde in einer afrikanischen Studie durch eine HAART im letzten Trimenon sowie sechs Monate nach der Geburt trotz Stillen die Transmissionsrate <1% gesenkt. In der „Mma Bana“-Studie, die in Kollaboration mit der Harvard Universität in Boston und der botswanischen Regierung durchgeführt wurde, erhielten 560 schwangere Frauen mit ≥200 CD4-Zellen/µl entweder ab der 26.-34. Schwangerschaftswoche AZT/3TC/ABC oder LPV/r plus AZT /3TC und 170 Frauen mit <200 CD4-Zellen/µl ab der 18.-34. Schwangerschaftswoche NVP plus AZT/3TC wie es die botswanischen Leitlinien empfehlen. Die Transmissionsprophylaxe der Kinder bestand aus einer Einzeldosis Nevirapin gleich nach der Geburt und im ersten Monat nach der Geburt täglich AZT. Unabhängig vom Therapieregime erreichten durchschnittlich 95% der Frauen vor der Geburt und 93% während des Stillens eine Viruslast von <400 HIV-RNA-Kopien/ml. Von den 790 Lebendgeburten wurden 669 Kinder gestillt. Die kumulative Transmissionsrate betrug bis sechs Monate nach der Geburt <1% und während der Stillzeit traten nur zwei vertikale Transmission auf (0,3%). Die Kindersterblichkeit betrug 3% und unterschied sich in den drei Studienarmen nicht (Shapiro R et al. WELBB1).
Sex macht glücklich…
Irgendwie haben wir es ja alle schon geahnt, dass Sex glücklich macht – auch HIV-positive Menschen. Das Center for Excellence in HIV/AIDS im kanadischen Vancouver wollte es jedoch genau wissen und hat 457 HIV-Positive nach ihrem Sexualleben befragt. 55% der Teilnehmer, gaben an, in den letzten sechs Monaten vor der Befragung Sex gehabt zu haben. 70% davon waren schwul oder bisexuell, 47% heterosexuelle Männer und 49% heterosexuelle Frauen. Die sexuelle Aktivität korrelierte mit „eine Beziehung haben”, einem besseren Körperbild und besseren Sexualfunktionen sowie besseren Werten für fast alle Aspekte der Lebensqualität. Wer hätte das gedacht… (Mtambo A et al. MOPEC015)
DART
DART (Development of AntiRetroviral Therapy in Africa) ist die bislang größte afrikanische Therapiestudie, in der eine Vielzahl von Fragen untersucht werden, die nicht nur für Afrika relevant sind. Eine der interessanten Fragen war die nach dem Nutzen der Steuerung der antiretroviralen Behandlung mittels CD4-Zahl und Basislabor im Vergleich zu rein klinischen Parametern.
An DART nehmen 3.316 therapienaive Erwachsene in Uganda und Simbabwe teil, die Daten werden in England ausgewertet. Bei den Patienten im WHO-Stadium 2, 3 und 4 bzw. einer CD4-Zahl <200/µl wurde eine ART eingeleitet. Drei Viertel erhielten initial AZT/3TC plus TDF. Die übrigen Patienten wurden in einer Substudie nach Randomisierung mit AZT/3TC plus Nevirapin (16%) oder plus Abacavir (9%) behandelt.
Wie nützlich sind Laborkontrollen?
Nach Einleiten der ART wurden die Patienten nach Randomisierung entweder nur klinisch (CDM) oder zusätzlich durch Laboruntersuchungen (LDM) überwacht. Alle wurden monatlich von einer Schwester bei der Medikamentenausgabe gesehen und mussten sich alle drei Monate beim Arzt melden. Allen Patienten wurde alle drei Monate Blut abgenommen. Im CDM-Arm wurden die CD4-Zahl nie bzw. eine Anämie oder Lebertoxizität nur bei Grad 4 weitergeleitet. Die Patienten im CDM-Arm wurden beim Auftreten eines WHO-Ereignisses Grad 4 umgestellt, im LDM-Arm zusätzlich anhand der CD4-Zahl.
Im Vergleich zu Studien aus Industrieländern waren die afrikanischen Patienten deutlich jünger (36 Jahre) und häufiger Frauen (66%). Der Immundefekt war weiter fortgeschritten. 33% hatten eine CD4-Zahl <50/µl, 23% AIDS und 55% WHO-Stadium 3 (d.h. typische Symptome wie orale Candidiasis, Gewichtsverlust, chronische Diarrhoe, TBC usw.).
Kein Unterschied bei Nebenwirkungen
Nach im Mittel
fünf Jahren waren in beiden Gruppen nahezu gleich viele Patienten am Leben (87%
vs 90%). Neue Ereignisse traten häufiger im CDM-Arm auf (459/28% vs 356/22%).
Das Fehlen der Laborparameter erhöhte das Risiko von WHO-Ereignis Grad 4 oder
Tod um rund 30%. Die absolute Differenz war jedoch gering. Sie betrug 1,7 pro
100 Personenjahre (p=0,0001), wobei der Unterschied erst nach dem zweiten Jahr
signifikant wurde (Abb. 1). Das heißt, um einen Todesfall zu verhindern,
müssten 130 Patienten ein Jahr lang regelmäßig untersucht werden.
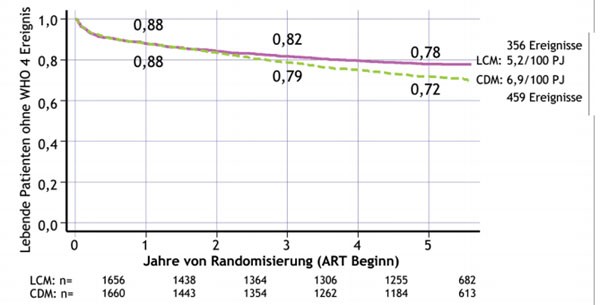
Abb. 1: Progression zu neuen WHO 4 Ereignissen oder Tod
(Primärer Endpunkt)
Im Hinblick auf die übrigen Laborparameter (Blutbild, Kreatinin, Transaminasen) bestand kein signifikanter Unterschied zwischen den beiden Gruppen sowohl im Hinblick auf schwere Nebenwirkungen als auch auf Umstellungen aufgrund von Laborparametern (Abb. 2). Nach vier Jahren waren noch 80% der Patienten auf der Firstline und über 60% nahmen immer noch das erste Regime ein. AZT/3TC war lediglich bei 6 bzw. 7% der Patienten, die dritte Substanz bei 10 bzw. 11% ersetzt worden. 22 bzw. 19% waren auf eine Secondline-Therapie umgestellt worden.
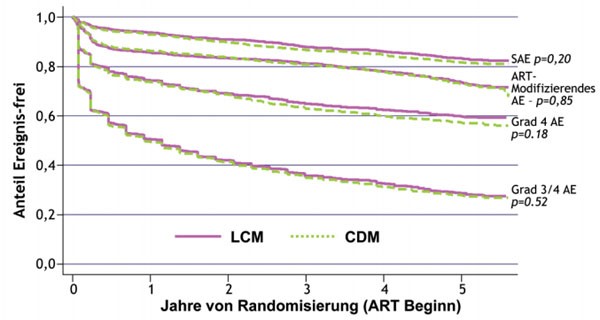
Abb. 2: Nebenwirkungen
In Afrika nicht kosteneffektiv
Die Implementierung von routinemäßigen Laboruntersuchungen (CD4-Zahl U5 und Basislabor U9 per annum) war trotz der geringeren Häufigkeit von Umstellungen auf ein Zweitlinien-Regime nicht kosteneffektiv – zumindest angesichts der aktuellen Preise für das Labor. Nach Worten des Studienleiters James Hakim, Universität Simbabwe, können ein Drittel mehr Patienten behandelt werden, wenn man lediglich die CD4-Zahl ab dem dritten Jahr kontrolliert. Die Frage nach der Viruslast, die in den letzten beiden Jahren zunehmend diskutiert wird, kann diese Untersuchung allerdings nicht beantworten (Mugyenyi P et al. TuSS103; Medina-Lara A et al. TuSS104).
Erhaltungstherapien
Das alte Konzept der Deeskalation hat in Kapstadt durch drei neue Studien wieder Aufwind bekommen (Vergl. Beitrag M. Stoll S. 23-25). In allen drei Studien wurden seit längerem optimal supprimierte Patienten ohne virologisches Versagen in der Vorgeschichte umgestellt. In der AIRES-Studie wurden mehr als 500 Patienten nach einer 36wöchigen Behandlung mit geboostertem Atazanavir (300 mg/100 mg) auf ungeboostertes Atazanavir (400 mg) jeweils in Kombination mit Abacavir/Lamivudin umgestellt oder gleich weiterbehandelt. 48 Wochen nach dem Switch waren in beiden Gruppen gleich viele Patienten immer noch komplett supprimiert (86% vs 81%, p=0,140) (Abb. 3), wobei das ungeboosterte Regime auch bei Patienten mit hoher Ausgangsviruslast gleichermaßen erfolgreich war. Lediglich bei einem Patienten kam es unter ungeboostertem Atazanavir zum bestätigten virologischen Versagen, bei dem eine NRTI-Mutation, aber keine primäre PI-Mutation nachgewiesen wurde. Vorteil der Umstellung waren ein günstigeres Lipidprofil und weniger Probleme mit Ikterus (4% vs 10%) (Squires K et al. WeLBB 103).
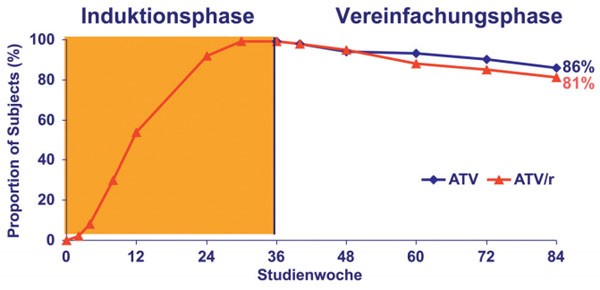
Abb. 3: AIRES: Anteil der Patienten mit einer Viruslast
<50 Kopien/ml, randomisierte Patienten (ITT-E, TLOVR)
Darunavir/r-Monotherapie
In zwei weiteren Studien wurden Patienten auf eine Darunavir/r-Monotherapie umgestellt. In der europäischen MONET-Studie waren es 256 Patienten, die mindestens sechs Monate komplett supprimiert waren und noch nie Darunavir eingenommen hatten. Sie wurden entweder mit einer Triple-Therapie (die NRTI konnten zu diesem Zeitpunkt optimiert werden) oder allein mit DRV/r (800/100 mg) OD weiterbehandelt. 80% der Patienten waren Männer, 90% weiß, das Alter betrug im Mittel 43 Jahre. Die CD4-Zellzahl lag bei 575/µl, die mittlere Therapiedauer betrug sieben Jahre.
Nach 48 Wochen lag die Viruslast bei gleich vielen Patienten immer noch unter der Nachweisgrenze (ITT 84 vs 85%, PP 88 vs 86%) (Abb. 4). Blips (meist zwischen 50 und 400 Kopien/ml) waren unter der Monotherapie häufiger. Alle Patienten, die nach zweimaliger konsekutiver Viruslast >50 Kopien/ml wieder NRTI erhielten, waren unter der Triple-Therapie erneut optimal supprimiert. Jeweils ein Patient pro Arm entwickelte Proteasehemmer-Mutationen. Vorteile der Umstellung war hier erneut ein geringerer Cholesterinspiegel (Arribas J et al. TuAb106).
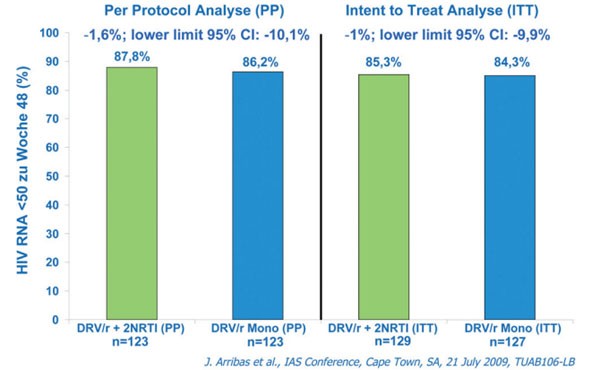
Abb. 4: MONET: Anteil der Patienten mit einer Viruslast
<50 Kopien/ml zu Woche 48, TLOVR, S = F
MONOI-ANRS
In der zweiten Studie, der französischen MONOI-Studie, die vom ANRS gesponsort wurde, erhielten 242 vorbehandelte Patienten mit einer Viruslast <400 Kopien/ml für mindestens sechs Monate und mit <50 Kopien/ml bei Studienbeginn, zunächst acht Wochen lang DRV/r (meist mit 1.200/ 200 BID) plus 2 NRTI. Anschließend wurden 225 Patienten nach Randomisierung entweder nur mit DRV/r 800/100 oder der bisherigen Therapie weiterbehandelt.
Rund drei Viertel der Patienten waren Männer, das Alter betrug 46 Jahre und die CD4-Zahl lag bei 600/µl. Die Patienten waren im Schnitt acht Jahre vorbehandelt, 40% waren 3-Klassen-erfahren. Therapieversagen war definiert als eine zweimal konsekutive Viruslast >400 Kopien/ml.
Nach 48 Wochen hatten in der ITT-Analyse 92% unter Triple-Therapie und 87,5% unter DRV/r-Monotherapie eine Viruslast <50 Kopien/ml. Damit wurde die Nicht-Unterlegenheit knapp verfehlt. In der Per-Protocoll-Analyse war die DRV/r-Monotherapie allerdings nicht unterlegen (99% vs 94,1%) (Abb. 5). Drei Patienten entwickelten unter der Monotherapie ein Therapieversagen. Einer davon hatte einen niedrigen Darunavir-Spiegel im Blut als Hinweis auf eine mangelhafte Adhärenz. Darunavir-assoziierte Mutationen wurden nicht beobachtet und bei allen Patienten führte die Zugabe von NRTI zur kompletten Suppression.
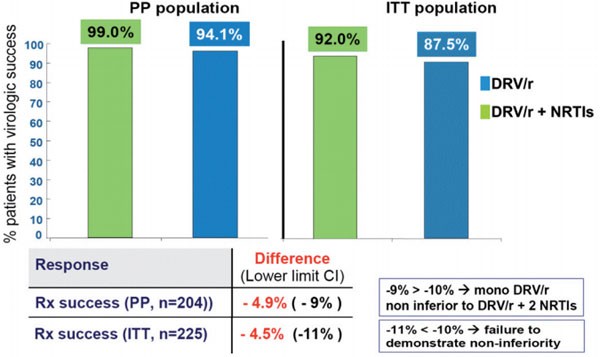
Abb. 5: MONOI Anteil der Patienten mit einer Viruslast
<50 Kopien/ml zu Woche 48
Problem: Liquorgängigkeit
Die Verträglichkeit der beiden Regime war vergleichbar. Unter Darunavir-Mono wurde bei einem Patienten eine HIV-Enzephalitis, bei einem anderen neurologische Symptome beobachtet. Ein Zusammenhang mit der Studienmedikation, d.h. mit einem geringeren „ZNS-Schutz“ bei Fehlen der NRTI, ist möglich (Katlama C et al. WeLBB102).
ARTEN: Nevirapin vs ATV/r
In der offenen ARTEN-Studie wurden rund 600 therapienaive Patienten mit NVP OD oder BID oder ATV/r jeweils in Kombination mit TDF/FTC behandelt. Primärer Endpunkt der Studie war nicht wie sonst üblich TLOVR (Time to loss of virologic response), sondern ein strengerer Endpunkt, nämlich gemäß den Empfehlungen der Europäischen AIDS-Gesellschaft (EACS) der Anteil der Patienten mit einer Viruslast <50 Kopien/ml nach sechs Monaten. Die übliche TLOVR-Analyse wurde als Sensitivitätsanalyse eingesetzt.
Vergleichbare Wirksamkeit
Unter Nevirapin OD sowie BID und ATV/r erreichten vergleichbar viele Patienten eine Viruslast <50 Kopien/ml zu Woche 24 und Woche 48 und auch Patienten mit hoher Viruslast sprachen gleichermaßen gut an (Abb. 6). Nebenwirkungen waren im Allgemeinen gleich häufig, wobei erwartungsgemäß Hautausschläge unter NVP und ein Ikterus unter ATV/r häufiger beobachtet wurden. Bei den Lipiden hatte NVP keinen Einfluss auf die Triglyceride, während ATV/r diese um rund 30% erhöhte. Das günstige HDL-Cholesterin stieg unter NVP stärker an, Gesamtcholesterin und das ungünstige LDL-Cholesterin waren unter ATV/r geringer (Soriano V et al. LBPEB07).
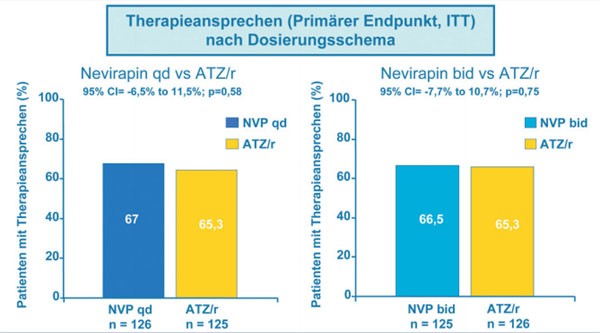
Abb. 6: Nevirapin qd und bid gleich wirksam
LPV/r OD vs BID bei Therapieversagen
Ob Lopinavir/Ritonavir OD auch bei Patienten mit Therapieversagen gleich wirksam ist wie LPV/r BID, wurde in der offenen Studie M06-802 an 599 vorbehandelten Patienten geprüft. Die Patienten waren Lopinavir-naiv, hatten im Schnitt eine PI-Mutation und der Prüfer beurteilte LPV/r als aussichtsreiche Kombination. Die Viruslast unter der „alten“ Therapie lag bei rund 4.000 Kopien/ml, die CD4-Zahl bei 254/µl und die Patienten wurden entweder mit LPV/r OD oder BID plus zwei NRTI behandelt.
Nach 48 Wochen hatten vergleichbar viele Patienten eine Viruslast <50 Kopien/ml (OD vs BID: 55% vs 52%) und zwar auch Patienten mit ein bis zwei PI-Mutationen. Bei Patienten mit drei und mehr Mutationen waren es 38% vs 57%, wobei allerdings die Patientenzahl (4/13 vs 8/14) so gering war, dass eine statistisch zuverlässige Aussage nicht möglich ist. Nebenwirkungen wie Diarrhoe (14% vs 11%) und Lipiderhöhungen (7% vs 5%) sowie die Abbruchrate wegen Nebenwirkungen (5% vs 7%) waren vergleichbar. Lediglich die Adhärenz war bei einmal täglicher Gabe signifikant besser (Zajdenverg R et al. TuAb104).
ABC – doch kein erhöhtes kardiovaskuläres Risiko?
Die Diskussion, ob Abacavir das kardiovaskuläre Risiko erhöht, geht weiter. Auf der CROI 2008 waren erstmals Daten aus der D:A:D-Studie präsentiert worden, die auf ein erhöhtes Myokardinfarktrisiko während der letzten sechs Monate einer Abacavir-Therapie hinwiesen. Mittlerweile liegen Analysen anderer Studien und Kohorten vor mit widersprüchlichem Ergebnis. Die auf der IAS-Konferenz präsentierten Daten zeigen kein erhöhtes Risiko. Vielmehr deutet die retrospektive Analyse der amerikanischen Veteranen-Kohorte (76.376 Personenjahre) auf einen sogenannten Channeling Bias für Nierenerkrankungen hin. Ohne Adjustierung für Nierenfunktionsstörungen, die ein wichtiger kardiovaskulärer Risikofaktor sind, erhöht Abacavir das Risiko für Ereignisse. Nach Berücksichtigung der Nierenerkrankung ist dagegen weder das Infarkt- noch das Schlaganfallrisiko erhöht (Abb. 7) (Bedimo R et al. MoAb202). Ferner waren die Entzündungsparameter (C-reactives Protein, Monocyte chemotractant protein-1, Osteoprotegrin, Adiponectin, IL-6, IL-10, Tumournekrosefaktor-alpha, ICAM-1, VCAM-1, Selectin E and P, D-dimer und Insulin) in der spanischen BICOMBO-Studie, in der Patienten mit einer Viruslast unter der Nachweisgrenze entweder auf Abacavir/Lamuvudin oder Tenofovir/Emtricitabin umgestellt wurden, nach einem Jahr nicht verändert (Martinez E et al. MoAb203).
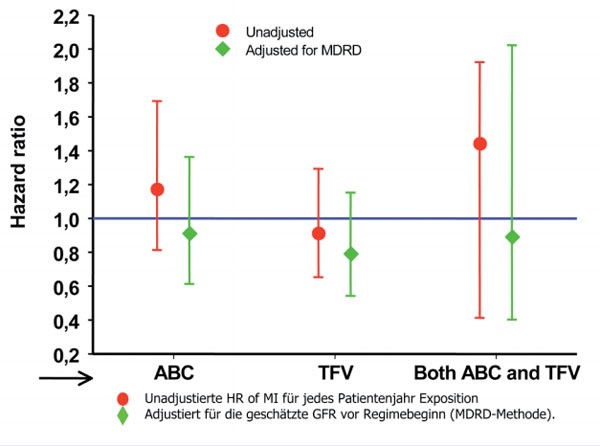 Abb. 7: Veteranen-Kohorte: ABC vs TDF im letzten Regime und
Infarktrisiko
Abb. 7: Veteranen-Kohorte: ABC vs TDF im letzten Regime und
Infarktrisiko
Neuer vielversprechender Integrasehemmer
Der neue Integrasehemmer
S/GSK1349572 bzw. GSK-572 der zweiten Generation hat die größte bisher bekannte
antivirale Potenz, wirkt auch gegen Raltegravir-resistente Isolate und muss nur
einmal täglich gegeben werden. In einer Phase-2a-Studie an 35 Patienten senkte
GSK-572 die HIV-Viruslast innerhalb von 10 Tagen um maximal -2,5 log. 70% der
Patienten unter 50 mg GSK-572 erreichten eine Viruslast <50 Kopien/ml und 90% <400 Kopien/ml. Die CD4-Zahl stieg um
15-106/µl. Die Verträglichkeit war gut. Kopfschmerzen waren die häufigsten
Nebenwirkungen. Die Phase-2b-Studien werden
in Kürze anlaufen (Lalezari J et al. TuAb105; Sato A et al. WePeA097; Underwood
M et al. WePeA098; Min S et al. WePeA09; Song I et al. WePeB250).
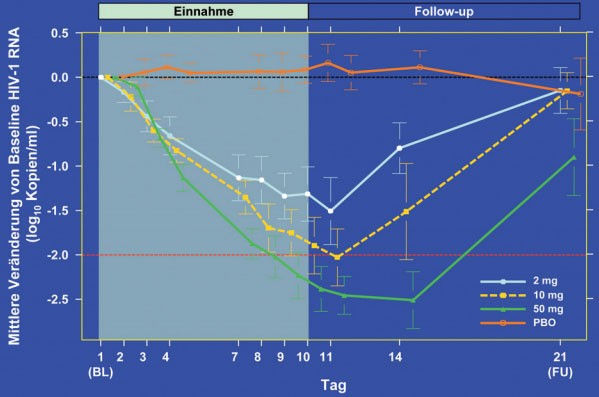
Neuer Integrasehemmer
S/GSK1349572 (GSK-572)










 Diese Seite weiter empfehlen
Diese Seite weiter empfehlen
