Eva Grützner Und Rika Draenert, München
Immundefekt bei HIV
Natürlicher Verlauf der HIV-Infektion
Zu
Beginn der HIV-Pathogenese infiziert das HI-Virus Zellen des
menschlichen Immunsystems, die den CD4-Oberflächenmarker tragen
(Langerhans Zellen, dendritische Zellen, T-Lymphozyten). Zum Andocken
und Eintritt in die Zielzelle benötigt das Virus zusätzlich den
CCR5-Corezeptor, den CD4 T-Zellen, Makrophagen und Mikrogliazellen im
Gehirn aufweisen. Mit Hilfe dieser Zellen gelingt es dem Virus, sich
zu vermehren und sich im Blut, in den lymphatischen Organen und im
ZNS auszubreiten. Durch Aktivierung zytotoxischer T-Zellen (CD8
T-Lymphozyten) des erworbenen Immunsystems, die virusinfizierte
Zellen zerstören können, erreicht die Anzahl der Viren einen Peak,
der häufig eine Million Viruskopien pro ml Blut übersteigt. Das
Abfallen und Einpendeln der Viruslast auf ein bestimmtes, individuell
unterschiedliches Niveau (viraler Setpoint) gilt als Prädiktor für
das Fortschreiten der Erkrankung ins Stadium AIDS.1
Es folgt eine asymptomatische Phase der Infektion, die 8 bis 10 Jahre
andauern kann. Abhängig vom Alter des Patienten, der Pathogenität
des Virus und anderen Umweltfaktoren kann diese Zeit sehr viel kürzer
sein (bis hin zu
weniger
als 1 Jahr).2
Trotz HIV-spezifischer Immunantwort besteht fortwährend virale
Replikation und die Viruslast bleibt auf dem erreichten Niveau. Ohne
Therapie geht die Kontrolle des Immunsystems über die
HIV-Replikation verloren (Phase der Progression; AIDS). Die CD4
T-Zellen nehmen ab, Pathogene können nicht mehr kontrolliert werden
und opportunistische Infektionen
treten auf (nach Appay3,
Simon4).
Es gibt allerdings Patienten, die deutlich langsamer als der Durchschnitt in der Phase der Progression ankommen. Diese Patienten sind wissenschaftlich sehr interessant. Unbehandelte Patienten in der asymptomatischen Phase mit einer Viruslast unter 2.000 Kopien/ml Blut werden als Controller bezeichnet.2 Weniger als ein Prozent der Patienten hat in der asymptomatischen Phase eine nicht nachweisbare Viruslast (<50 Kopien/ml) – sogenannte „elite controller“. Patienten, die eine normale CD4-Zellzahl (>400 Zel-len/µl) über mehr als 10 Jahre aufrecht erhalten (5-15%), werden als Long-term-non-progressors (LTNP) bezeichnet.1, 5-7
CD4 T-Lymphozyten
CD4 T-Lymphozyten sind ein essentieller Bestandteil der erworbenen (= adaptiven) Immunantwort. Die Anzahl der CD4 T-Zellen im gesunden Menschen beträgt ca. 500 bis 1.200 Zellen/µl Blut. Nach ihrer Reifung im Thymus wandern die naiven T-Zellen in die Lymphknoten ein und differenzieren zu verschiedenen Untergruppen aus. Am längsten bekannt sind Th1- und Th2-T-Zellen. Weitere im Moment bekannte Untergruppen sind z.B. Th17-, regulatorische (Treg)- und follikuläre T-Zellen.
Nach Kontakt mit Antigenfragmenten, die vom MHC-II-Komplex (= major histo-compatibility complex) präsentiert werden, werden naive CD4 T-Zellen spezifisch aktiviert. Sie unterstützen das Immunsystem bei seiner Aufgabe, Krankheitserreger zu bekämpfen und sorgen damit für eine immunologische Kontrolle der HIV-Virusreplikation.8, 9 Dabei haben sie folgende Funktionen: Erstens aktivieren sie die CTL Vorläuferzellen (s. CD8 T-Zellen), so dass eine primäre Immunantwort möglich ist und Gedächtniszellen gebildet werden.10, 11 Zweitens leiten sie einsatzfähige CD8 T-Zellen an ihren Einsatzort. Die Antigenpräsentation der dendritischen Zellen aktiviert CD4 T-Zellen IFNγ zu produzieren, was wiederum durch Chemokinbildung im epithelialen Gewebe, CD8 T-Zellen anlockt.12 Drittens steigern sie die humorale Immunantwort (B-Zellantwort und damit Bildung von Antikörpern).9, 13 Wie wichtig CD4 T-Zellen für eine effektive Immunantwort sind, zeigt sich auch im Tiermodell. So zeigten Battegay et al. und von Herrath et al. an CD4 defizienten knock out Mäusen, dass es diesen an ausreichender CD8-Immun-antwort und damit auch Viruskontrolle mangelte.13, 14
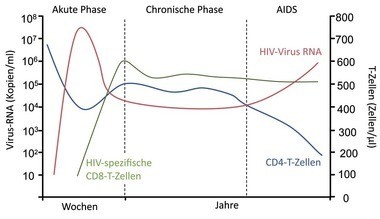
Abb. 1 Modell des natürlichen Verlaufs der HIV-Erkrankung (nach Simon 20064). Die Viruslast nimmt in den ersten Wochen der akuten Phase der Infektion stark zu. Die CD4 T-Zellen nehmen durch die Infektion ab. Nach Einsetzen der CD8-Immunantwort, wird ein Peak in der Viruslast erreicht, sie sinkt und pendelt sich auf ein bestimmtes Niveau ein. Nach einer Latenzphase kommt es ohne Therapie zu AIDS und Tod.
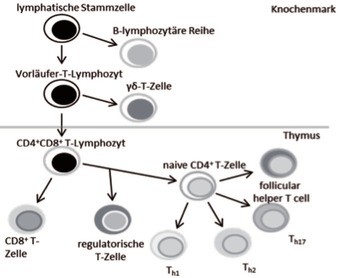
Abb. 2 Entwicklung der T-Lymphozyten. Die Vorläufer-T-Zelle entsteht im Knochenmark, wohingegen die weitere Entwicklung der T-Zellen im Thymus geschieht. Nach der Abspaltung der CD8 T-Zellen, differenzieren die CD4 T-Zellen in die verschiedenen Untergruppen aus.
Durch die anhaltende Virusreplikation nimmt die Zahl der CD4 T-Zellen im Laufe der HIV-Infektion kontinuierlich ab. Dies bedeutet, dass die beschriebenen Funktionen nicht mehr ausgeübt werden können – weder zur Kontrolle der HIV-Virämie noch zur Bekämpfung von opportunistischen Erregern. Der Verlust der CD4 T-Zellen stellt den Hauptfaktor des Immundefekts in der HIV-Infektion dar.
CD8 T-Lymphozyten
Eine zweite Gruppe von T-Zellen, die im Thymus reifen, tragen vorwiegend den CD8 Oberflächenmarker. CD8 T-Zellen sind zytotoxische Zellen, die Peptid-MHC-I-Komplexe erkennen und u.a. virusinfizierte Zellen, die virale Peptide im MHC-I Komplex präsentieren, lysieren. CD8 T-Zellen brauchen die Hilfe der CD4 T-Zellen, um aktiviert zu werden und an den Infektionsherd zu gelangen.15
Bereits 1986 wurde die Hemmung der HIV-Virusreplikation durch CD8 T-Lymphozyten in vitro entdeckt16 und 1987 wurden HIV-spezifische zytotoxische T-Lymphozyten in HIV-positiven Patienten nachgewiesen.17, 18 Die zentrale Rolle der HIV-spezifischen CD8 T-Zellen zeigt sich schon in der akuten Phase der Infektion. So steigt die Viruslast nur solange an, bis die zytotoxischen CD8 T-Zellen aktiviert sind und stark zunehmen, erreicht aufgrund der starken CD8-Immunantwort ihren Höhepunkt und fällt wieder ab (s. auch Abb.).19-23 Auch in der chronischen Phase kämpfen CD8 T-Lymphozyten kontinuierlich gegen das Virus.24, 25 Die CD8 T-Zellantwort ist anfänglich so stark und effektiv, dass das Virus gezwungen wird, in bestimmten genetischen Bereichen zu mutieren. Durch die Ausbildung der sogenannten Escape-(Flucht-)Mutationen v.a. in der akuten Phase, gelingt es dem Virus den Selektionsdruck zu umgehen und weiter zu replizieren.26-29 Heute ist klar, dass die CD8 T-Zellantwort im Laufe der Infektion ihre Effektivität verliert. Dieses Phänomen wird auch Immunerschöpfung genannt und ist eine weitere Facette des Immundefekts in der chronischen HIV-Infektion. Die Ursachen der Immunerschöpfung sind derzeit Gegenstand intensiver Forschung. Hierbei spielen sicherlich viele Faktoren eine Rolle, u.a. HIV selbst und die ausgeprägte Immunaktivierung (siehe unten) bei dieser Infektion. In den letzten Jahren wurden zudem inhibitorische Faktoren, darunter Rezeptoren (z.B. PD-1) und Zellen (z.B. myeloid-derived suppressor cells = MDSC), als Auslöser für die Immunerschöpfung identifiziert.
Immunaktivierung
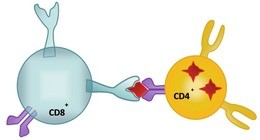
Abb. 3 Schematische Darstellung einer CD8 T-Zelle, die den Peptid-MHC-I-Komplex auf einer CD4 T-Zelle erkennt. Dies führt zur Zerstörung der infizierten CD4 T-Zelle.
Die
Aktivierung der Immunzellen ist ein physiologischer Prozess, der
essentiell für das Ablaufen einer Immunantwort ist. Sie wird über
Signalübertragungswege erreicht. Unter normalen Bedingungen wird
die Immunaktivierung wieder
beendet und nach Entfernung des Pathogens stirbt ein Großteil der
pathogenspezifischen T-Zellen. Der Rest wird zu
Gedächtniszellen.
In der HIV-Infektion kommt es zu einer übermäßigen, chronischen Immunaktivierung, die nicht wieder beendet wird. Dadurch ist der T-Zellturnover erhöht30, polyklonale B-Zellen werden aktiviert31, die T-Zellen mit aktiviertem Phenotyp nehmen zu32 und die Spiegel an proinflammatorischen Cytokinen und Chemokinen steigen an.33 Auch CD8 T-Zellen werden kontinuierlich aktiviert, um die Virusreplikation adäquat zu hemmen. Die Frage hinsichtlich der Ursache und Wirkung dieser gesteigerten Immunaktivierung, ob nun also das Virus die Immunaktivierung antreibt oder die Immunaktivierung die Virusreplikation, ist im Moment noch ungeklärt.34
Gemessen wird die Immunaktivierung auf Lymphozyten über den Marker CD38. Eine erhöhte Expression dieses Markers prognostiziert ein schnelleres Fortschreiten der chronischen HIV-Infektion zu AIDS und Tod, und dies sogar besser als z.B. die CD4-Zellzahl.35 Daneben besteht auch ein Zusammenhang zwischen einem kürzerem Überleben bei fortgeschritten erkrankten Patienten und einer erhöhten T-Zellaktivierung.36 Patienten unter einer erfolgreichen ART, bei denen die Immunaktivierung gemessen an der Expression des Markers CD38 nicht abnahm, wiesen einen niedrigeren CD4-Anstieg auf.37, 38 Somit stellt die chronische, pathologische Immunaktivierung in der HIV-Infektion eine wichtige Komponente des Immundefekts dar.
Bedeutung von medikamentöser Immunsuppression
Begleiterkrankungen
machen es teilweise notwendig, den bereits bestehenden Immundefekt
aufgrund der HIV-Infektion durch eine Therapie zu verstärken. Die
HIV-Infektion geht mit einem erhöhten Risiko für Malignome einher.
Hierzu gehören vor allem die infektions-assoziierten Tumoren, wie
z.B. das Kaposi-Sarkom (HHV-8 assoziiert) und das Non-Hodgkin-Lymphom
(EBV-assoziiert).44
Dass der Immundefekt bei HIV-Erkrankung zur Entstehung der Tumoren
beiträgt, zeigt die Tatsache, dass das Risiko für diese Malignome
mit Beginn einer HAART wieder sinkt.44
Für die häufigsten HIV-assoziierten Malignome, nämlich die
Lymphome, gibt es gute Daten und auch Empfehlungen.45
Insgesamt sollten HIV-Infizierte genauso behandelt werden wie
HIV-negative mit vergleichbar hohen Remissions- und Überlebensraten.
HAART sollte von Anfang an initiiert oder weitergeführt werden unter
Berücksichtigung der pharmakologischen Interaktionen. Da
Ritonavir-geboostete Proteaseinhibitor (PI)-Regime die Toxizität der
Chemotherapeutika teils signifikant steigern können, werden heute –
wenn möglich – Integraseinhibitor (INI)-basierte Regime
empfohlen.45
Die Kombination von Chemotherapie mit HAART kann zwar den CD4-Verlust
durch die Chemotherapie nicht verhindern, jedoch kommt es unter HAART
zu einer schnelleren Erholung der CD4-Zellzahl.46
Hier muss natürlich je nach absoluter CD4-Zellzahl an die primäre
und sekundäre Prophylaxe von opportunistischen Infektionen gedacht
werden.47
Die Empfehlungen für andere maligne Erkrankungen als Lymphome sind
analog: Therapie wie bei Nicht-Infizierten und Beginn oder
Fortsetzung der HAART.47
Eine Studie untersuchte die Kombination von Raltegravir-basierter
HAART mit Chemotherapie für ganz unterschiedliche Tumoren. Hierbei
zeigte sich, dass diese Regime sicher und effektiv bei allen
Patienten waren.48
Insgesamt bedeutet eine Chemotherapie eine generelle Immunsuppression
und trifft bei HIV-Infizierten häufig auf niedrige
Helferzellzahlen. Aufgrund
des kombinierten Immundefekts wird auch immer eine Therapie dieser
Patienten in Zentren mit ausgewiesener Erfahrung empfohlen.
Zu Tumor-Nekrose-Faktor alpha (TNFα)-Blockern in der HIV-Infektion gibt es deutlich weniger Daten als zur konventionellen Chemotherapie. Es gibt Fallberichte u.a. zu Morbus Crohn, reaktiver Arthritis und rheumatischen Erkrankungen.49, 50 Eine Fallserie berichtet von acht Patienten mit therapie-refraktären rheumatischen Erkrankungen und HIV-Infektion. Hierbei war die Anwendung von Infliximab, Etanercept oder Adalimumab wirksam und sicher bei Patienten mit einer CD4-Zellzahl >200/µl und einer Viruslast <60,000 Kopien/ml.51 Dieses Ergebnis wird durch weitere Fallserien unterstützt.52 Wenn also die HIV-Infektion zu Beginn der Therapie mit TNFα-Blockern eine Kontraindikation darstellte, so ist dies zumindest für HIV-Infizierte mit gutem Immunstatus zu revidieren. Wie bei HIV-negativen Patienten, kann es auch in diesem Patientengut zu einer Reaktivierung der Tuberkulose kommen.53
Lebendimpfungen
Lebendimpfungen bringen das Risiko mit, dass es bei Patienten mit primärem oder sekundärem Immundefekt zu einer generalisierten Erkrankung mit dem Impfvirus kommen kann. Hierzu gibt es bei HIV-Infizierten tatsächlich Fallberichte, z.B. über eine generalisierte Windpockenerkrankung als Erstmanifestation einer HIV-Infektion nach Varizellen-Impfung.54 Eine genauere Untersuchung des Virus ergab, dass die Erkrankung durch den Oka-Impfvirus ausgelöst war. Man muss also einerseits vorsichtig sein, um den Patienten keinem Risiko auszusetzen. Andererseits ist auch klar, dass der Schutz vor Masern, Mumps, Röteln oder Varizellen entweder durch stattgehabte Infektion oder Impfung z.B. in der HIV-infizierten Bevölkerung Österreichs relativ häufig fehlt.55 Ähnliche Daten werden im Moment für Deutschland erhoben (C. Schwarze-Zander, persönliche Kommunikation). Zudem verlaufen die Erkrankungen bei Immundefekt schwerer, was dafür spricht, dass diese Patienten geimpft sein sollten. Für die Masern-Mumps-Röteln (MMR)-Impfung gibt es eine Studie, die zeigt, dass die Impfung bei Kindern unter HAART gut vertragen wurde.56 Im Moment läuft eine Studie des Deutschen Zentrums für Infektionsforschung (DZIF), die die Sicherheit und Verträglichkeit der MMR-Impfung bei erwachsenen HIV-Patienten in Deutschland untersucht. Für die Gelbfieberimpfung gibt es eine Metaanalyse, die die Gelbfieberimpfung bei 484 HIV-Patienten untersuchte. Insgesamt war die Impfung sicher und produzierte eine gering niedrigere Immunität als bei HIV-negativen. Höhere CD4-Zellzahlen und niedrigere Viruslasten waren entscheidend für die Ausbildung protektiver Antikörpertiter.57 Dementsprechend empfehlen die europäischen Leitlinien, dass die MMR-, Varizellen- und Gelbfieberimpfung nur bei einer CD4-Zellzahl <200/µl (14%) und/oder AIDS kontraindiziert ist (EACS Guidelines 7.1 2014). Die orale Typhus- und die orale Polioimpfung ist immer kontraindiziert, da es Totimpfstoffe als Alternative gibt (EACS Guidelines 7.1 2014).
Ausblick
Auch mehr als 30 Jahre seit der Ausbreitung der HIV-Infektion bleibt der HIV-induzierte Immundefekt und seine Folgen weiter ein großes Forschungsfeld. Die Aufnahme der Immunaktivierung in das 7 Punkte Programm zur globalen Strategie der Internationalen AIDS Gesellschaft (IAS) mit dem Ziel, eine Heilung58 zu erzielen, unterstreicht seine Bedeutung.










 Diese Seite weiter empfehlen
Diese Seite weiter empfehlen
