Hendrik Streeck, Essen
Warum wir einen HIV Impfstoff brauchen
Es ist anzunehmen, dass ein Impfstoff, der 86% Schutz vor einer HIV Infektion bietet, wahrscheinlich sofort zugelassen wird. Leider gibt es diesen Impfstoff noch nicht, aber es gibt die Möglichkeit der Präexpositionsprophylaxe (PrEP). Die tägliche Einnahme von Truvada (Tenofovir disoproxil/Emtricitabine) senkt das Risiko einer HIV Infektion im Durchschnitt um 86%. Wenn wir bereits jetzt einen so effektiven Schutz vor HIV durch eine PrEP erreichen können, warum brauchen wir dann noch einen HIV Impfstoff? Warum wird diese Form der Prophylaxe nicht wie ein „de facto“ Impfstoff betrachtet und weitmehr flächendeckend ausgegeben? Warum sehen einige Wissenschaftler und Ärzte die PrEP mit Skepsis, obwohl man eine HIV Infektion verhindern kann?
Es ist nicht zu leugnen, dass die PrEP wenn sie richtig und durchgängig angewendet wird, einen bemerkenswerten Schutz bietet, doch genau hier liegt auch die Problematik. Werden die Tabletten nicht regelmäßig eingenommen, verschwindet der Schutz. Vergesslichkeit ist menschlich, auch im Zeitalter von elektronischen „reminders“. Auch ist unser Körper nicht unfehlbar. So mag es beispielsweise sein, dass gastrointestinale Störungen, die Wirksamkeit von PrEP verringern. Diese kleinen, menschlichen Versehen können das HIV-Risiko entscheidend und nachhaltig erhöhen. Bei einem Kondom sieht man direkt, ob ein Schutz vorhanden oder eingerissen ist, bei Truvada® sieht man es nicht. Bei einem gerissenen Kondom kann man noch auf die Postexpositionsprophylaxe (PEP) zurückgreifen, bei der PrEP nicht.
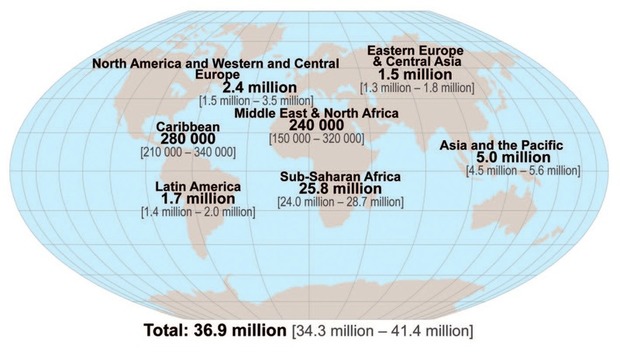
© UNAIDS
Mehr Resistenz?
Hinzu kommt, dass einige HI-Viren gegen Truvada® resistent sind und eine Infektion trotz der regelmässigen Einnahme des Medikaments auftreten kann. Diese resistenten Viren sind selten, dennoch mehren sich die Fälle von Infektionen unter PrEP. Vier Fälle sind derzeit bekannt. Jeder der Fälle wird hitzig in der Fachwelt diskutiert. Ob dies langfristig einen Einfluss auf die Viruspopulation hat und zum Beispiel der Anteil an Truvada®-resistenten Viren weltweit ansteigen wird, darüber herrscht unter Experten geteilte Meinung. Ein mathematisches Modell suggeriert, dass der Anteil resistenter Viren zunehmen wird. Eine andere Publikation besagt, dass es dauerhaft keine Veränderungen geben wird. Hier wird letztendlich nur eine genaue Beobachtung über einen längeren Zeitraum Aufschluss geben können.
Die PrEP ist also allenfalls eine Übergangslösung, um die HIV-Epidemie besser in den Griff zu bekommen und vor allem die zu schützen, die sich entweder nicht mit anderen Methoden selber schützen können oder nicht schützen wollen. Zusammengefasst also, das Risiko derer herunterzusetzen, die derzeit das höchste Risiko haben, sich mit HIV zu infizieren. Langfristig ist jedoch klar, dass nur ein HIV-Impfstoff die Epidemie beenden kann. In den letzten Jahrhunderten wurde deutlich, dass Impfstoffe die beste Waffe gegen einen Erreger sind, um eine Epidemie zu beenden. Pocken und Polio wurden durch konsequente Impfungen ausgerottet und nur noch wenige erkranken weltweit an anderen tödlichen Erkrankungen wie Masern, Mumps oder Tetanus.
Problem GP120
Die Idee der Impfung ist simpel. Durch das Einbringen eines weniger virulenten, abgetöteten Erregers oder Bestandteile eines Erregers, wird das Immunsystem ‚trainiert‘ und ‚lernt‘, wie es am besten mit infektiösen Erkrankungen umgeht. Nach diesen oder ähnlichen Mechanismen wurden bisher rund 35 Impfstoffe entwickelt und auf dem Markt zugelassen. Für HIV ist ein vergleichbares Verfahren indes nicht möglich. Weder ist es möglich, abgetötete HIV-Erreger als Impfstoff zu verwenden, noch kann das komplexe Oberflächenprotein gp120 des HI-Virus leicht im Labor nachgebaut werden.
Gp120 besteht aus drei Teilen, die ineinander verschränkt einen Hohlraum bilden. Diese 3D-Struktur zerfällt jedoch im Reagenzglas. Weiterhin suggerieren die gängigen cartoonhaften Darstellungen von HIV, dass es viele dieser gp120 Strukturen auf der Oberfläche des Virus gibt. Elektronenmikroskopische Untersuchungen haben jedoch gezeigt, dass ein HI-Virus im Durchschnitt nur zwölf dieser Strukturen besitzt. Der Rest der Membran von HIV besteht aus körpereigenen Zellmembranen und ist dadurch nicht für das Immunsystem erkennbar. Hinzu kommt, dass 50% des gp120 Molekül aus Zucker besteht. Menschen können aber sehr schlecht Immunantworten und vor allem keine Gedächtnisantworten gegen Zucker bilden. Dies mag evolutionär bedingt sein, da unser AB0 Blutgruppensystem aus Zucker besteht. Eine starke bleibende Immunantwort dagegen, würde zu vielen Totgeburten führen, wenn die Mutter eine Gedächtniszellantwort gegen die fremde Blutgruppe ihrer Kinder gebildet hätte. Auch besitzt das Oberflächenmolekül gp120 eine sehr große Diversität, wodurch ein Impfstoff, der vielleicht gegen ein bestimmtes Virus wirksam ist, bei dem anderen vollkommen wirkungslos bleibt.
Problem Integration

© Who
Sobald HIV sich in das Genom der Wirtszelle eingeschrieben hat, meistens in das Genom einer CD4-Helferzelle, ist es nur noch schwer vom Immunsystem zu erreichen. Antikörper können das Virus so nicht mehr erkennen. Die Idee ist, dass dann die adaptive CD8-T-Zell-antwort die infizierten Zellen erkennen und abtöten könnte. Leider hat bislang kein Impfstoff, der auf CD8-T-Zellantworten basiert vor einer Infektion geschützt weder im Affenmodel noch in klinischen Studien. Verstecken, variabel zu sein, sich mit nicht-erkennbaren Strukturen zu umgeben und Teil der Zellmaschinerie zu werden, macht HIV zu einem komplizierten Gegner.
Zarte Hoffnung
Daher ist es überraschend, dass nach vielen Jahren der Misserfolge ein HIV-Impfstoff 2009 in Thailand eine 30%-ige Effektivität zeigte. Das bedeutet, dass eine von drei geimpften Personen durch den Impfstoff geschützt war (ALVAC+ALVAC/AIDSVAX-RV144Ttrial). Mehr noch, im ersten Jahr nach der Impfung lag der Schutz bei rund 60%. Interessanterweise blieben aber die durch den Impfstoff induzierten Immunantworten nicht erhalten und so verschwand auch der Schutz vor der HIV-Infektion innerhalb eines Jahres. Trotzdem wurde damit eins bewiesen: ein HIV-Impfstoff ist möglich.
Der Erfolg des RV144 Impfstoffes kam insofern überraschend, da man in der Fachwelt nach jahrelangem Theoretisieren eher pessimistisch gestimmt war, nicht zuletzt, weil zuvor ein anderer Impfstoff sogar vorzeitig gestoppt wurde, da sich mehr Teilnehmer am Ende in der Impfstoffgruppe im Vergleich zu der Plazebogruppe infiziert haben (Step-Trial). Natürlich hatte der Impfstoff im Step-Trial die freiwilligen Teilnehmer nicht infiziert, er hat aber das Immunsystem sensibilisiert, so dass wahrscheinlich mehr Zielzellen für HIV in der Mukosa zur Verfügung standen. Das negative Ergebnis der Step-Studie wurde nochmal in der HVTN505 Studie zwei Jahre später bestätigt, so dass dieses Impfkonzept eines Adenovirus 5 (Ad5) Vektors erstmal nicht weiterverfolgt wird.
Mehrere Dutzend Impfkonzepte wurden bereits im Menschen auf ihre Sicherheit und die induzierten Immunantworten in Phase I Studien getestet. Es fehlt also nicht an Ideen, aber der Möglichkeit diese Ideen auf ihre Effektivität zu testen. Diese letzte Phase der Testung (Phase III) ist aufwendig und teuer, da mehrere tausend HIV-negative Freiwillige eingeschlossen und über Jahre beobachtet werden müssen.
Neue Studie am Start
Welche Impfstoffkonzepte könnten es in diese letzte, aufwendige Phase schaffen? Die Hoffnungen ruhen derzeit noch auf Bestandteilen des RV144 Trials. Zurzeit wird eine Variante des RV144 Trial in mehreren klinischen Zentren in Südafrika getestet (HVTN702). Es ist allerdings nicht eine genaue Wiederholung des vorherigen Impfstoffes, sondern wichtige Bestandteile wurden ausgetauscht. Der Kanarienpocken-Vektor ALVAC vom Subtyp B wurde durch einen Subtyp C ersetzt, da der Subtyp C in Südafrika prävalent ist. Ob dies einen Einfluss hat, ist ungewiss. In Thailand wurde der Subtyp B getestet, wobei dort der HIV Subtyp AE dominiert. Weiterhin ist das gp120 Booster-Protein nicht A244 AIDSVAX, sondern ein neues bivalentes Subtyp C Protein. Auch ein anderes Adjuvanz wird benutzt. Wo in RV144 Aluminiumhydroxid benutzt wurde, wird im neuen Versuch das Adjuvanz MF59 verwendet.
Kontroverse Diskussion
Diese vielen Veränderungen des Studiendesigns werden kritisch diskutiert, da am Ende nicht genau gesagt werden kann, welche Veränderung einen positiven oder negativen Effekt hatte. Besonders kontrovers wird der Wechsel zum Adjuvant MF59 gesehen. Der RV144 Impfstoff wurde im Vorfeld mit beiden Adjuvanzien, Aluminiumhydroxid oder MF59, an Rhesusaffen getestet. Interessanterweise zeigte die Originalformulierung den gleichen 30%igen Schutz, wohingegen die neue Formulierung mit MF59 keinerlei Schutz zeigte. In einer vorangegangenen Analyse zu der neuen Phase-3-Studie HVTN702 zeigte der Impfstoff genügend Immunogenität, jedoch macht seitdem den Wissenschaftlern Sorge, dass einige der induzierten Immunantworten sehr viel niedriger sind, als es in RV144 beobachtet wurde. Diese Daten wurden erstmalig auf der HIV Research for Prevention (R4P) Konferenz vorgestellt, sind aber bis jetzt noch nicht veröffentlicht worden.
Neue Strategien
Langfristig liegen die Hoffnungen nicht nur auf RV144 basierten Impfkonzepten, sondern es werden weitere vielversprechende Impfstrategien (mehr als zwei Dutzend) derzeit in klinischen Phase-1-Studien getestet. So hat Robert Gallo, einer der Pioniere der HIV-Forschung, ein gp120-Protein entwickelt, das die Bindung von HIV an den CD4-Rezeptor nachstellt und dadurch konservierte Regionen des gp120 offenlegt. Dies ist interessant, da diese Regionen in Subtyp B, C und AE gleich sind und dadurch universaler als andere Impfstoffe wirken könnten. Weiterhin wird die Kombination von einem Adenovirus 26 (Ad26) mit einem modifiziertem Ankara Virus Vektor (MVA) getestet, was bei Rhesusaffen Erfolge erzielte. Auch andere Vektoren sind in Testung wie der Adenovirus 35 (Ad35) Vektor, der AAV Vektor, der Kanarienpocken Vektor NYVAC, CMV Vektor oder VSV Vektor. Alle diese Vektoren haben gemeinsam, dass sie genetisches Material von HIV in Zielzellen bringen und die Bestandteile von HIV durch die zelleigene Maschinerie exprimieren. Die Vektoren unterscheiden sich nicht nur dadurch, welches Material von HIV sie enthalten, sondern auch in der Art und Weise wie und durch welche Wege das neugebildete HIV-Material präsentiert wird. Hierdurch können unterschiedliche Wege des Immunsystems angesprochen werden und unterschiedliche Immunantworten ausgelöst werden. Wir wissen allerdings noch nicht, welche Immunantwort wir induzieren wollen. Das Prinzip der Impfung existiert bereits über Hunderte von Jahren hinweg und doch verstehen wir nur wenig, wie der Impfschutz tatsächlich entsteht. Dies mag sogar je nach Erreger sehr unterschiedlich sein. Während es bei anderen Erregern reichte, diese nur Abzutöten oder die Oberflächenstruktur nachzubauen, gibt es diese Möglichkeit bei HIV nicht. Daher wird viel getestet und probiert und letztendlich wird uns erst der Test im Menschen zeigen, ob wir den richtigen Impfstoff gefunden haben.










 Diese Seite weiter empfehlen
Diese Seite weiter empfehlen
