Christoph Stephan, Frankfurt
ART der Zukunft Neue Substanzen und Klassen in Sicht
Warum benötigen wir immer mehr Medikamente für die antiretrovirale Therapie? Heutzutage ist das Ziel einer HI-Virussuppression doch bei fast jedem Patienten und jeder Patientin mit guter Adhärenz zur antiretroviralen Medikation zu erreichen. Allerdings hat die Therapie in heutiger Zeit den unterschiedlichen Lebenswirklichkeiten zu folgen und nicht umgekehrt, wie z.B. in der Frühzeit der ART. Individualisierung ist das Schlüsselwort! Und nicht zu vergessen, darüber hinaus gibt es doch noch einige wenige stark vorbehandelte Patienten, die neue Medikamente zur Virussuppression oder zur Vereinfachung ihrer Therapie brauchen.
Noch in diesem Jahr
Seit nunmehr fast einem Jahrzehnt bilden die Integrase-Stranginhibitoren (INSTI) das Rückgrat moderner ART-Kombinationen. An dieser antiretroviralen Medikamentenklasse scheint auch in absehbarer Zukunft kein Weg vorbei zu führen. Neue INSTI-basierte Kombinationen kurz vor der Zulassung sind das Single-Tablet-Regime von Gilead Sciences Bictegravir/FTC/TAF (Biktarvy®) und als Switchoption die Fixkombination von ViiV Healthcare & Janssen: Dolutegravir/Rilpivirin (Juluca®). Am Horizont dahinter ist die intramuskulär zu verabreichende Therapie mit Cabotegravir und Rilpivirin in Sicht, die derzeit in einer Phase-3-Studie geprüft wird.
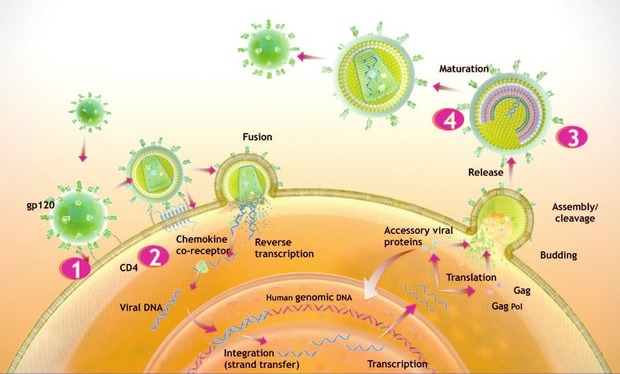
Abb.
1 Der HIV-Lebenszyklus und Angriffspunkte für die antiretrovirale
Therapie (ART): so wirken neue HIV-Medikamente – Ansatzpunkte von
Attachmentinhibitoren, z.B. Fostemsavir 1, weitere Entry-Inhibitoren,
z.B. Idalizumab 2, Capsid- 3 und Maturations-Inhibitoren 4
INSTI manchmal nicht
Aber:
auch der Einsatz von INSTIs kann individuell limitiert sein, z.B.
aufgrund von Resistenz nach Therapieversagen der ersten
Medikamentengeneration, namentlich bei Raltegravir-assoziiertem
virologischen Versagen, da diese Substanz eine relativ niedrige
Resistenzbarriere aufweist und somit anfällig für
Resistenzentwicklung ist, insbesondere wenn eine nicht-suppressive
antiretrovirale Therapiekombination über längere Zeit weitergeführt
wurde. Andere moderne INSTIs, namentlich Dolutegravir, weisen
manchmal neuropsychiatrische Nebenwirkungen auf, die Grund für einen
Therapieabbruch sein können.1
Die Monotherapie mit INSTIs bleibt weiterhin unrealistisch2,
hier werden auch in
Zukunft Kombinationspartner benötigt.
Auch die möglichen Therapiepartner von INSTI namentlich NRTI, NNRTI und PI können Probleme bereiten. Altbekannte Probleme sind neben Resistenzentwicklung und Unverträglichkeit metabolische Störungen und Langzeitnebenwirkungen.
Hinter‘m Horizont Fostemsavir
Fostemsavir (GSK3684934, früher BMS-663068) gehört zur Gruppe der „Entry-/Fusionsinhibitoren“ (Attachment-Inhibitor) und ist ein Prodrug des antiretroviralen Wirkstoffs „Temsavir“ (jetzt: GSK2616713). Erst nach Metabolisierung und Umwandlung des oral applizierbaren Fostemsavir in Temsavir wird eine frühe Kontaktaufnahme des HI-Virus mit der CD4-positiven Zelle verhindert. Temsavir blockiert die HIV-Bindungsstelle gp120 – also die „Noppe“ an der HIV-Außenhülle, mit der das Virus eine Bindung mit dem CD4-Rezeptor der menschlichen Zelle eingehen will, noch bevor es durch die CCR5- oder CXCR4-Korezeptor-Aktivierung zur Fusion von HIV und Zelle kommt.
Fostemsavir wurde zusammen mit der gesamten HIV-Entwicklungssparte der Firma Bristol-Myers Squibb verkauft an die Firma ViiV-Healthcare, hinter der die Firma GlaxoSmithKline (GSK) steht, die die Zulassung nun namentlich vorantreibt. Die multizentrische Phase 3-Studie, die voraussichtlich zur Zulassung als antiretrovirales Medikament führen wird, heißt BRIGHTE (GSK205888/früher: AI438-047) und das Studiendesign ist unter www.clinicaltrials.gov erläutert (siehe ebenda: NCT02362503).
Fostemsavir ist oral verfügbar und muss zweimal täglich eingenommen werden. Erste Ergebnisse der BRIGHTE-Studie wurden auf dem europäischen AIDS-Kongress in Mailand im Oktober 2017 präsentiert.3 Alles in allem scheint die Substanz bezüglich des Sicherheitsprofils akzeptabel zu sein, allerdings finden sich die eher mild ausgeprägten Nebenwirkungen relativ häufig: Übelkeit und Erbrechen, Kopfschmerz, allgemeine Schwäche und Diarrhoe, die allerdings in einer vulnerablen Studienpopulation beobachtet wurden. Die Studie wurde laut Protokoll an Patientinnen und Patienten mit weit fortgeschrittener Resistenz durchgeführt.
Fazit: Fostemsavir wird nach Zulassung eine interessante Option für stark vorbehandelte Patientinnen und Patienten sein, um auch diesen eine einfache, ggf. duale Therapieoption mit starken Kombinationspartnern, insbesondere INSTIs, zu ermöglichen und alte Mega-HAART-Kombinationen zu ersparen. Weitere Erkenntnisse aus Studien können aber im Verlauf vor und kurz nach Zulassung immer noch unliebsame Überraschungen ergeben.
Ibalizumab
Die Besonderheit von Ibalizumab (TMB-355 oder TNX-355) ist, dass es ein Vertreter der sogenannten „Entry Inhibitoren“ ist und gleichzeitig Potenzial für „Long-Acting“ hat. Die Substanz kann aufgrund einer Halbwertszeit von mehr als 3 Tagen im größeren Zeitabstand gegeben werden.
Ibalizumab ist ein monoklonaler Antikörper und kann folglich auch nur parenteral (intravenös, aber auch intramuskulär und subkutan) gegeben werden. Er richtet sich gegen die extrazelluläre Domäne des menschlichen CD4-Rezeptors4, blockiert also praktisch das Gegenstück zur Bindungsstelle des Attachment-Inhibitors Fostemsavir. Allerdings kann sich bei unzureichender HIV-1 Therapie ohne potente Kombinationspartner eine Resistenz in-vivo entwickeln. Es wurde die genotypische Entstehung von Mutationen in der variablen Region V5 beobachtet, die für das HIV-1 Hüllen-Glykoprotein verantwortlich ist, jedoch besteht wohl keine Kreuzresistenz mit dem schon 2003 zugelassenen Entry-Inhibitor Enfuvirtid (T20).5 Bereits 2003 wurden Ergebnisse einer Phase I-Studie präsentiert (als TNX-355) und obwohl immer noch nur aus einer Reihe von kleineren Studien Ergebnisse (zumeist einarmig oder Dosisfindung) als Kongresspublikationen (zum Beispiel6) und wenigen Journal-Vollpublikationen vorliegen, wurde Ibalizumab kürzlich von einer kleinen Biotech-Firma (TaiMed Biologics) in den USA als Trogarzo® (800 mg iv alle 14 Tage) zur Zulassung gebracht, für die Behandlung bei Multiresistenz.
Fazit: Eine spannende Therapieoption, auch weil die Kombination mit Fostemsavir aufgrund einer totalen Blockade des HIV-Zelleintritts auf beiden Seiten der gp120/CD4-Rezeptorinteraktion interessant sein könnte – nicht nur für die antiretrovirale Therapie, sondern auch für die HIV-Präexpositionsprophylaxe (PrEP). Die Probleme von monoklonalen Antikörpern (z.B. Inaktivierung des Medikaments durch Antikörperbildung) sollten allerdings noch sehr genau evaluiert werden. Wegen der parenteralen Applikation und des hohen Preises (in den USA 118.000 US$ pro Patient und Jahr) wird diese Substanz nur für wenige Patienten in Frage kommen, weshalb sie nicht nur die „Fast Track“-Zulassung, sondern auch den „Orphan Drug“-Status erhielt.
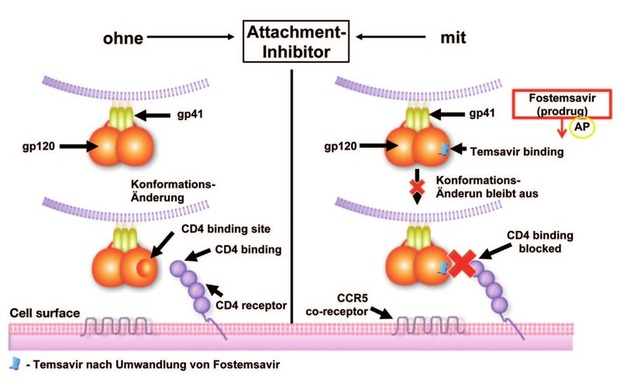
Abb. 2 Wirkungsmechanismus und -ort von Attachment-Inhibitoren (z.B. Fostemsavir)
Capsid-Inhibitor GS-CA1
Auf der amerikanischen Retroviruskonferenz (CROI) 2017 erregte ein Vortrag große Resonanz, der ein ganz neues Wirkprinzip als Therapieoption darstellte: die Präsentation des ersten Wirkstoffs der neuen Medikamentenklasse der Capsid-Inhibitoren. Eine aktuell durchgeführte Medline-Suche veranschaulicht das ganz frühe Entwicklungsstadium der Substanz GS-CA1, die bei der Firma Gilead angesiedelt ist: nur eine einzige Journal-Publikation findet sich Anfang März 2018 in der Medline.7
GS-CA1 ist der Prototyp der HIV-Kapsid-Funktionsinhibitoren. Der Eingriff in den Lebenszyklus von HIV geschieht spät, wenn sich nach Durchlaufen der intrazellulären Replikation das Virus bereits wieder extrazellulär aufhält und im Ausreifungsprozess das Viruskapsid formiert. Die Schädigung der Kapsidformation lässt das Virion als nicht infektionsfähig zurück. Das deutet eine hohe antiretrovirale Potenz an – weitgehend unabhängig von Subtypen7 und vorhandenen (erworbenen) HIV-Resistenzmutationen in anderen antiretroviralen Medikamentenklassen. Außerdem besteht aufgrund pharmakologischer Eigenschaften das Potenzial für eine „Long-Acting“-Substanz.
Fazit: Die Mitteilung zu GS-CA1 aus der frühen Medikamentenentwicklung zeigt: immer noch wird geforscht und die antiretrovirale Kombinationstherapie weiterentwickelt.
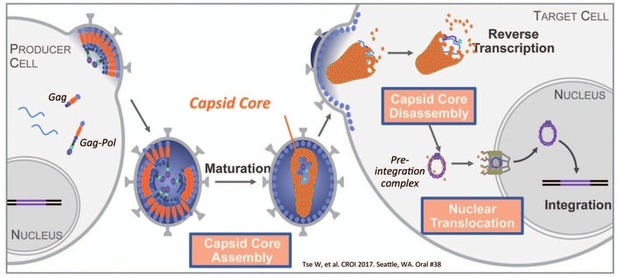
Abb. 3 Neuer potenter HIV-Kapsid-Inhibitor (GS-CA1) mit Potenzial als „Long-acting”
Maturationsinhibitoren
Noch ein letztes Wort zur Medikamentenklasse der Maturationsinhibitoren (z.B. Beviramat, BMS-955176, GSK8232), die ähnlich dem soeben besprochenen Capsidinhibitor (GS-CA1) in einen ganz späten Schritt der HI-Virusausreifung eingreifen. Sie blockieren nach Durchlaufen des intrazellulären Replikations-zyklus die „Reifung“ des schon extrazellulären Virus.
Hier
gibt es schon geraume Zeit Kandidaten in der Entwicklung: Wirkstoff
der ersten Medikamentengeneration war
Beviramat, das die
Zulassung allerdings nicht mehr anstrebt, nachdem klar ist, dass
abhängig vom HIV-Subtyp eine ausgeprägte intrinsische Resistenz
bestehen kann.8,9
Das Entwicklungsprogramm von BMS-955176 wurde nach Verkauf von
Bristol-Myers Squibb an ViiV. Healthcare (GlaxoSmithKline) nicht
fortgeführt.10
Ob der andere Zweitgenerations-Maturationsinhibitor aus der
GSK-eigenen Entwicklung GSK8232, je die Zulassungsreife erreichen
wird, ist dem Autor dieses Beitrags unbekannt.
Fazit: Es bleibt unklar, ob die Medikamentenklasse der Maturationsinhibitoren jemals für die Therapie zur Verfügung stehen wird. Dennoch ist zu hoffen, dass diese interessante Option für neue Kombinationen genutzt wird und die aufwändige Zulassung nicht allein marktwirtschaftlichen Gründen zum Opfer fällt.
Referenzen:
1 Hoffmann C, Welz T, Sabranski M, Kolb M, Wolf E, Stellbrink HJ, Wyen C. Higher rates of neuropsychiatric adverse events leading to dolutegravir discontinuation in women and older patients. HIV Med. 2017 Jan;18(1):56-63
2 Blanco JL, Oldenbuettel C, Thomas R, et al. Pathways of resistance in subjects failing dolutegravir monotherapy. In: Program and abstracts of the 2017 Conference on Retroviruses and Opportunistic Infections; February 13-16, 2017; Seattle, WA, USA. Abstract 42. Foundation for Retrovirology and Human Health, Alexandria, VA, USA
3 Kozal M, Aberg J, Pialoux G, et al. Phase 3 study of fostemsavir in heavily treatment-experienced HIV-1-infected participants: Day 8 and Week 24 primary efficacy and safety results (BRIGHTE study, formerly 205888/AI438-047). European AIDS Conference; October 25-27, 2017; Milan, Italy.
4 Jacobson JM, Kuritzkes DR, Godofsky E, et al. Safety, Pharmacokinetics, and Antiretroviral Activity of Multiple Doses of Ibalizumab (Formerly TNX-355), an Anti-CD4 Monoclonal Antibody, in Human Immunodeficiency Virus Type 1-Infected Adults. Antimicrob Agents Chemother 2009;53(2):450-7.
5 Bruno CJ, Jacobson JM. Ibalizumab: an anti-CD4 monoclonal antibody for the treatment of HIV-1 infection. J Antimicrob Chemother. 2010 Sep;65(9):1839-41.
6 Weinheimer
S, Marsolais C, Cohen Z, Lewis S. Long-acting ibalizumab
susceptibility in multi-drug resistant HIV patients. Abstract
presented at: International AIDS Society (IAS) Conference on HIV
Science; July 23-26, 2017; Paris, France. Available at:
http://programme.ias2017.org/Abstract/Abstract/
4685. Last
accessed on March 3rd, 2018.
7 Perrier M, Bertine M, Le Hingrat Q et al. Prevalence of gag mutations associated with in vitro resistance to capsid inhibitor GS-CA1 in HIV-1 antiretroviral-naïve patients. JAC 2017;72:2954-5.
8 Adamson CS, Sakalian M, Salzwedel K et al. Polymorphisms in Gag spacer peptide 1 confer varying levels of resistance to the HIV-1maturation inhibitor bevirimat. Retrovirology 2010; 7: 36
9 LuW, Salzwedel K,Wang D et al. A single polymorphism in HIV-1 subtype C SP1 is sufficient to confer natural resistance to the maturation inhibitor bevirimat. Antimicrob Agents Chemother 2011; 55: 3324-9
10 GSK
discontinues development of maturation inhibitor BMS-955176.
Available
at: http://i-base.info/htb/30865 – Last accessed on March 3rd, 2018











 Diese Seite weiter empfehlen
Diese Seite weiter empfehlen
