Susanne Buder, Klaus Jansen, Berlin
Update Gonorrhoe Neisseria gonorrhoeae in Zeiten des Superbugs
Infektionen mit N. gonorrhoeae stellen weltweit und in Deutschland aufgrund ihrer Häufigkeit, möglicher Folgeerkrankungen und der Resistenzsituation ein besorgniserregendes Problem dar. Die Diagnostik und Therapie auf Basis der Leitlinien ist von entscheidender Bedeutung für den adäquaten Umgang mit dem Erreger auf individueller wie kollektiver Ebene.
Epidemiologie
Die Gonorrhoe, im Volksmund auch Tripper genannt, ist eine sexuell übertragbare Infektion (STI), die durch Neisseria gonorrhoeae verursacht wird. Nach den aktuellen Schätzungen der WHO für das Jahr 2012 stellt die Gonorrhoe mit weltweit 78,3 Mio. neuen Erkrankungsfällen pro Jahr die vierthäufigste sexuell übertragbare Erkrankung nach Trichomoniasis, Chlamydien-Infektionen und genitalen Warzen dar.1 Geschätzt werden 35,2 Millionen Erkrankungsfälle in der Region Westpazifik, 11,4 Millionen in der Region Südostasien, 11,4 Millionen in der Region Afrika, 11,3 Millionen in der Region Amerika, 4,7 Millionen in der Region Europa und 4,5 Millionen im östlichen Mittelmeerraum.1-3 In Deutschland sind Infektionen mit N. gonorrhoeae mit Ausnahme von Sachsen nicht meldepflichtig. In Sachsen hat sich die Inzidenz der 2017 gemeldeten Infektionen mit 21,2/100.000 Einwohner im Vergleich zu 2007 verdoppelt.4 Hierfür sind sicherlich nicht nur eine ansteigende Krankheitsdynamik, sondern auch Verbesserungen der Testangebote verantwortlich. Daten aus anderen Ländern legen allerdings auch einen realen Anstieg von Infektionen nahe. Die regionalen Meldezahlen aus Sachsen lassen sich nicht direkt auf die gesamtdeutsche Situation übertragen. Die erneute Einführung einer Meldepflicht für Infektionen mit N. gonorrhoeae in Deutschland wird daher aufgrund der hohen Relevanz des Erregers, auch im Hinblick auf Antibiotika-Resistenzen (s.u.), angestrebt.
Neue WHO-Strategie
Im Jahr 2016 beschloss die Weltgesundheitsversammlung der Vereinten Nationen (UN) die WHO-Strategie für sexuell übertragbare Infektionen 2016-2021. Eines der Hauptziele ist eine weltweite Verringerung der Häufigkeit von Gonokokken-Infektionen um 90%.5 Um das zu erreichen, können zwei wesentliche Aufgaben formuliert werden:
- Verbesserung des diagnostischen Vorgehens zum Nachweis von N. gonorrhoeae und der Bestimmung der antimikrobiellen Empfindlichkeit
- adäquates Therapie- und Krankheitsmanagement der Gonorrhoe bei antimikrobieller Resistenz.
Aktuelle Resistenzsituation
Die Antibiotikaresistenz (AMR) bei N. gonorrhoeae stellt ein globales Problem für die Behandlung und Kontrolle der Gonorrhoe dar. In den letzten Jahren wurde die Gefahr eines potentiell kaum therapierbaren, hochresistenten Erregers (multidrug-resistant N. gonorrhoeae, MDR-NG, und extensively drug-resistant N. gonorrhoeae, XDR-NG) weltweit sehr ernst genommen. So hat die WHO N. gonorrhoeae 2017 als Erreger mit hoher Priorität eingestuft, für den aufgrund einer besorgniserregenden Resistenzsituation neue Antibiotika dringend benötigt werden. Gegenüber allen Antibiotika, die bisher zur Behandlung eingesetzt wurden, konnten Resistenzen nachgewiesen werden.6
Derzeit ist Ceftriaxon als injizierbares Cephalosporin der 3. Generation mit erweitertem Spektrum in den meisten Ländern die einzige noch verbliebene empirische Monotherapie bei Gonorrhoe. Allerdings finden sich weltweit Fallberichte über einzelne Therapieversagen und Resistenzen gegenüber Cephalosporinen der 3. Generation.7-10 Daher wird in den meisten Therapieguidelines eine duale antimikrobielle Therapie, hauptsächlich Ceftriaxon plus Azithromycin, empfohlen.11,12
Neben high-level Resistenzen werden zunehmend auch Multiresistenzen beobachtet. Aus Großbritannien und Australien wurde Anfang 2018 von XDR-NG Isolaten mit kombinierter high-level Resistenz für Azithromycin (MHK >256 mg/L) und Resistenz für Ceftriaxon (MHK 0,5 mg/L) berichtet, welche zu Therapieversagen von Ceftriaxon im Pharynxbereich führte. Die Infektionen waren reiseassoziiert und wurden in Südostasien erworben.13-15 Im Januar 2019 berichtete Public Health England von zwei weiteren Fällen mit gleichzeitiger Resistenz gegen Ceftriaxon und Azithromycin, welche jedoch in Europa erworben wurden. Eine erhöhte Aufmerksamkeit bei der Behandlung der Gonorrhoe gegenüber der lokalen und globalen Resistenzsituation ist daher dringend erforderlich.
Deutsche Daten
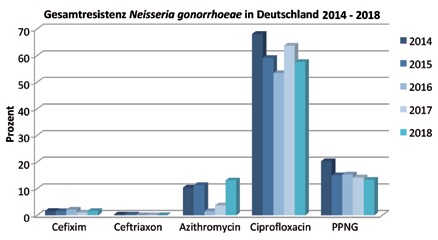
Abb. 1 GORENET – Resistenzsurveillance für N. gonorrhoeae, 2014-2018 (in Prozent)
Quelle: Konsiliarlabor für Gonokokken
Um diese Entwicklungen für Deutschland zu bewerten, sammelt das Gonokokken-Resistenz-Netzwerk (GORENET) als nationale N. gonorrhoeae – Resistenzsurveillance des Robert Koch-Instituts und des Konsiliarlabors für Gonokokken seit 2014 bundesweit Isolate und Daten von Empfindlichkeitstestungen (Abb. 1). Die Daten aus dem GORENET dienen auch als Evidenzbasis für die Formulierung der jeweils aktuellen Therapieleitlinien.
Hierbei zeigt sich für das derzeit als first-line Therapeutikum eingesetzte Ceftriaxon die Resistenzlage in Deutschland mit 0,5% resistenten Stämmen stabil. Jedoch ist eine wechselnd starke Resistenzentwicklung gegenüber Azithromycin mit bis zu 12% resistenter Stämme zu beobachten. Zudem kommt es zur Ausprägung von high-level Azithromycin-resistenten N. gonorrhoeae-Stämmen (MHK >256 mg/L), welche in Großbritannien sogar zu einem Ausbruch mit über 50 Fällen führte.16
Die Resistenzraten gegenüber weiteren Antibiotika, wie Ciprofloxacin (53-71%) und Penicillin (15-29%) lagen in Deutschland in den Jahren 2014-2018 sehr hoch. Für Tetrazyklin gibt es keine kontinuierlichen Surveillancedaten, da es auch hier bei weit verbreiteten Resistenzphänotypen nicht mehr zur Behandlung der Gonorrhoe empfohlen werden kann. Internationale Publikationen berichten über Resistenzraten von 20-100%.17,18 Im Rahmen der GORENET-Surveillance 2018 lag die Rate bei 80% (n=214). Damit können diese antimikrobiellen Substanzen die von der WHO geforderten Heilungsraten von 95% bei weitem nicht erreichen.
Klinisches Bild
Abb. 2 Reinkultur Neisseria gonorrhoeae

Abb. 3 Epsilomertest zur Bestimmung der Antibiotikaempfindlichkeit
Der Mensch ist der einzige Wirt von N. gonorrhoeae. Die Übertragung erfolgt ausschließlich durch Schleimhautkontakt. Im Vordergrund stehen die Symptome der Schleimhautinfektion an der Eintrittspforte und mögliche lokale Komplikationen. Neben der klassischen, symptomatischen Urethritis sind auch Infektionen von Rektum, Pharynx und Konjunktiven zu berücksichtigen. Die Komplikationen der Gonorrhoe betreffen Frauen besonders stark und umfassen aufsteigende Infektionen mit pelvic inflammatory disease (PID), ektopische Schwangerschaften und Unfruchtbarkeit sowie eine erhöhte Wahrscheinlichkeit für den Erwerb und die Weitergabe von HIV.7, 19-20
Disseminierte Gonokokkeninfektionen (DGI), mit der klassischen Trias undulierende Fieberschübe, akute Polyarthritis und akrale vaskulitische Hauterscheinungen, sind selten, werden jedoch auch wegen oligosymptomatischer Verläufe vermutlich häufiger übersehen. Im vergangenen Jahr kam es unter dem therapeutischen Einsatz monoklonaler Antikörper mit der Bindung an Protein C5 der Komplementkaskade vermehrt zu Fallberichten von DGI.21
Das klinische Spektrum der Gonorrhoe wird durch eine große Zahl asymptomatischer Krankheitsverläufe (ca. 50%) ergänzt.22 Trotz fehlender klinischer Symptomatik sind die Erreger virulent und können zu symptomatischen Infektionen bei Kontaktpersonen führen. Insbesondere die Gonokokken-Pharyngitis verläuft in ca. 90% der Fälle asymptomatisch.22,23 Zudem hat der Pharynx als Kompartiment zum genetischen Austausch zwischen N. gonorrhoeae und apathogenen, kommensalen Neisserien und anderen Bakterienspezies große Bedeutung, da hier vermutlich die meisten Resistenzen erworben werden.24 Asymptomatische Infektionen stellen wesentliche Infektionsreservoire dar, welche in die diagnostischen (Abstrichentnahme aus allen potentiell infizierten anatomischen Regionen) und therapeutischen Erwägungen (regionale Wirkspiegel bestimmter Antibiotika) einbezogen werden müssen.
Diagnostik
Die Diagnose einer Gonorrhoe erfolgt durch Erregernachweis in der Kultur oder mittels Nukleinsäure-Amplifikationstechniken (NAAT). Die NAAT-Diagnostik ist deutlich sensitiver als die Kulturdiagnostik25 und sowohl symptomatische als auch asymptomatische Infektionen lassen sich sensitiv nachweisen. Zudem sind NAAT-basierte Tests in der klinischen Praxis wenig aufwendig und es können auch vom Patienten selbst gewonnene Proben genutzt werden. N. gonorrhoeae ist ein genetisch sehr variables Bakterium mit der Fähigkeit zur Aufnahme und zum Austausch von DNA und der Ausbildung von Mutationen. Diese Tatsache spielt bei der Entwicklung von Antibiotika-Resistenzen eine entscheidende Rolle. Sie hat auch Bedeutung für die Erregerdiagnostik mittels NAAT, da bei einer genetisch veränderten Zielregion die Sensitivität eines molekularbiologischen Diagnostik-Tests reduziert sein kann.26-29
Die breite Anwendung molekularer Tests bei der Diagnostik der Gonorrhoe führt jedoch zunehmend zur Vernachlässigung der kulturellen Erregerdiagnostik und dadurch zu einem Mangel an Empfindlichkeitstestungen und Informationen zur antimikrobiellen Resistenz. Dabei ist bekannt, dass die weit verbreitete antimikrobielle Resistenz in hoch-variablen Stämmen von N. gonorrhoeae das Management und die Kontrolle von Gonorrhoe stark beeinträchtigt und es daher, z.T. auch subklinisch, zu Misserfolgen in der Therapie kommt. Es ist deshalb neben der Probenentnahme für eine NAAT-basierte Diagnostik immer ein zusätzlicher Abstrich für die kulturelle Empfindlichkeitstestung durchzuführen.
Therapieerfolgskontrolle
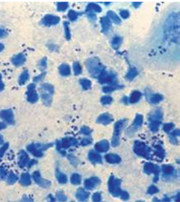
Abb. 4 Direktpräparat Urethritis durch N. gonorrhoeae (Methylenblaufärbung)
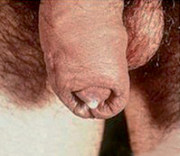
Abb. 5 Der sogenannte „Bonjour-Tropfen“
©Foto: CDC
Eine Therapieerfolgskontrolle wird nach jeder Behandlung einer Gonorrhoe empfohlen. Sie sollte bei NAAT-Diagnostik frühestens 4 Wochen nach Therapieende durchgeführt werden, da NAAT nicht zwischen lebenden und abgestorbenen Mikroorganismen unterscheiden können und hier die Diagnostik von residualer DNA vermieden werden sollte.28,29 Die Kontrolluntersuchung sollte alle Regionen, die für eine Infektion in Frage kommen (urethral, rektal, pharyngeal), berücksichtigen.
Therapie
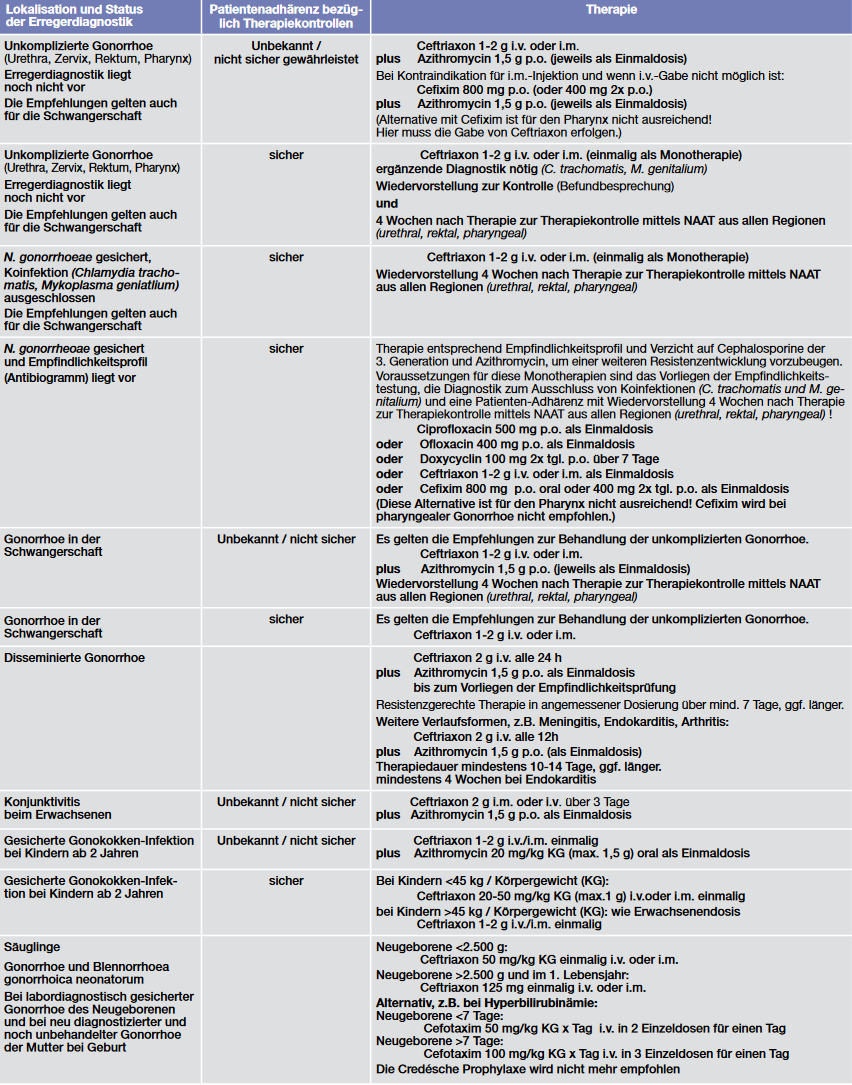
Aufgrund der weit verbreiteten antimikrobiellen Resistenz bei N. gonorrhoeae, der Persistenz der AMR-Determinanten im Erreger und der Nichtverfügbarkeit von diagnostischen Tests, die AMR-Ergebnisse direkt zum Zeitpunkt des Behandlungsbeginns liefern, müssen Ärzte auf eine empirische Behandlung von Gonorrhoe zurückgreifen. Eine aktualisierte S2K-Leitlinie zur „Diagnostik und Therapie der Gonorrhoe“ wurde von der DSTIG in Zusammenarbeit mit 15 weiteren Fachgesellschaften erstellt und Anfang 2019 durch die AWMF veröffentlicht. Eine ausführliche Übersicht zur Therapie der Gonorrhoe in Abhängigkeit von der Lokalisation der Infektion und des Patientenkollektivs bietet Tabelle 1.29
Die Leitlinie empfiehlt derzeit für die kalkulierte Behandlung der unkomplizierten Gonorrhoe ein duales Therapieregime aus Ceftriaxon 1-2 g i.v. oder i.m. in Kombination mit Azithromycin 1,5 g p.o. jeweils einmalig.
Bei adhärenten Patienten (z.B. Schwangerschaftsbetreuung, Spezialambulanzen oder hausärztliche Konsultationen) kann eine Monotherapie mit Ceftriaxon 1-2 g i.v. oder i.m. einmalig durchgeführt werden, um ggf. eine Übertherapie sowie eine weitere Resistenzzunahme gegen Azithromycin zu vermeiden. Dies gilt auch für Patienten mit nachgewiesener isolierter N. gonorrhoeae-Infektion. Eine Wiedervorstellung muss hierbei gewährleistet sein, um eine Therapieerfolgskontrolle durchzuführen und ggf. eine mögliche Koinfektion mit C. trachomatis oder M. genitalium nachfolgend behandeln zu können.
Nur in Ausnahmefällen
Nur in Ausnahmefällen, in denen die i.v.- oder i.m.-Gabe von Ceftriaxon nicht erfolgen kann, sollte auf das oral applizierbare Cephalosporin Cefixim in einer Dosierung von 800 mg p.o. einmalig (oder 2x 400 mg p.o.), zurückgegriffen werden, da Cefixim nach Beobachtungen der letzten Jahre für eine kalkulierte Therapie nur noch eingeschränkt empfohlen werden kann.
Zum einen kommt es zur Ausprägung von Resistenzen, zum anderen werden aufgrund der Pharmakokinetik keine ausreichenden Spiegel des Medikaments in Pharynx und Rektum erreicht und somit keine sichere Behandlung gewährleistet. Auch hier muss an eine duale Therapie mit Azithromycin gedacht werden, wenn keine Patientenadhärenz besteht.
Penicillinallergie
Bei einer Penicillinallergie (ß-Lactamallergie) kommt primär Azithromycin 2 g p.o. einmalig als Einzeltherapeutikum zum Einsatz. Bei diesem Regime muss unbedingt die Durchführung einer Empfindlichkeitstestung und eine Therapieerfolgskontrolle erfolgen.
Liegen Ergebnisse einer Empfindlichkeitstestung vor, sind Cephalosporin- und Azithromycin-sparende Regime zu favorisieren, um einer Resistenzentwicklung gegenüber diesen first-line-Antibiotika vorzubeugen. Absolute Voraussetzungen für diese Monotherapien sind der Ausschluss von Koinfektionen und eine gegebene Patienten-Adhärenz.
1 Newman L, Rowley J, Vander Hoorn S et al. Global Estimates of the Prevalence and Incidence of Four Curable Sexually Transmitted Infections in 2012 Based on Systematic Review and Global Reporting. PLoS One. 2015 Dec 8;10(12):e0143304.
2 Cole MJ, Spiteri G, Jacobsson S et al. Overall Low Extended-Spectrum Cephalosporin Resistance but high Azithromycin Resistance in Neisseria gonorrhoeae in 24 European Countries, 2015. BMC Infect Dis. 2017 Sep 11;17(1):617.
3 Wi T, Lahra MM, Ndowa F et al. Antimicrobial resistance in Neisseria gonorrhoeae: Global surveillance and a call for international collaborative action.PLoS Med. 2017 Jul; 14(7): e1002344.
4 Landesuntersuchungsanstalt Sachsen. Jahresbericht 2017 der Landesuntersuchungsanstalt Sachsen - Tabellenteil. Dresden: Landesuntersuchungsanstalt für das Gesundheits- und Veterinärwesen Sachsen; 2018.: file:///C:/Users/drsus/AppData/Local/Temp/JB_2017_Sachbericht.pdf
5 World Health Organization (WHO). Global health sector strategy on sexually transmitted infections 2016–2021: Towards ending STIs Geneva: WHO; 2016. Available from: http://www.who.int/reproductivehealth/publications/rtis/ghss-stis/en/
6 World Health; Organization (WHO). Global surveillance network for gonococcal antimicrobial susceptibility Geneva: WHO; 1990. WHO/VDT/90-452. Available from: http://apps.who.int/medicinedocs/documents/s16348e/s16348e.pdf
7 World; Health Organization (WHO). Global action plan to control the spread and impact of antimicrobial resistance in Neisseria gonorrhoeae Geneva: WHO; 2012. Available from: http://www.who.int/reproductivehealth/publications/rtis/9789241503501/en/
8 Unemo M, Shafer WM. Antimicrobial resistance in Neisseria gonorrhoeae in the 21st Century: Past, evolution, and future. Clin Microbiol Rev. 2014; 27(3):587-613.
9 Unemo M. Current and future antimicrobial treatment of gonorrhoea–the rapidly evolving Neisseria gonorrhoeae continues to challenge. BMC Infect Dis. 2015; 15:364.
10 Cole MJ, Spiteri G, Jacobsson S et al.Overall Low Extended-Spectrum Cephalosporin Resistance but high Azithromycin Resistance in Neisseria gonorrhoeae in 24 European Countries, 2015. BMC Infect Dis. 2017 Sep 11;17(1):617.
11 Weston EJ, Workowski K, Torrone E, et al. Adherence to CDC Recommendations for the Treatment of Uncomplicated Gonorrhea - STD Surveillance Network, United States, 2016. MMWR Morb Mortal Wkly Rep. 2018 Apr 27;67(16):473-476.
12 Brooks B, Patel R; European Collaborative Clinical Group (ECCG). The 2012 International Union against Sexually Transmitted Infections European Collaborative Clinical Group report on the diagnosis and management of Neisseria gonorrhoeae infections in Europe. Int J STD AIDS. 2013 Jun;24(6):419-22.
13 “UK case of Neisseria gonorrhoeae with high-level resistance to azithromycin and resistance to ceftriaxone acquired abroad” https://www.gov.uk/government/publications/multi-drug-resistant-gonorrhoea-in-england-2018.
14 Eyre DW, Sanderson ND, Lord E et al. Gonorrhoea treatment failure caused by a Neisseria gonorrhoeae strain with combined ceftriaxone and high-level azithromycin resistance, England, February 2018. Euro Surveill. 2018 Jul;23(27).
15 Whiley DM, Jennison A, Pearson J, Lahra MM. Genetic characterisation of Neisseria gonorrhoeae resistant to both ceftriaxone and azithromycin. Lancet Infect Dis. 2018 Jul;18(7):717-718.
16 Fifer H, Cole M, Hughes G et al. Sustained transmission of high-level azithromycin-resistant Neisseria gonorrhoeae in England: an observational study. Lancet Infect Dis. 2018 May;18(5):573-581.
17 https://www.cdc.gov/std/stats16/gonorrhea.htm
18 Scott HM, Klausner JD. Sexually transmitted infections and pre-exposure prophylaxis: challenges and opportunities among men who have sex with men in the US. AIDS Res Ther. 2016 Jan 19;13:5.
19 Cohen MS, Hoffman IF, Royce RA et al. Reduction of concentration of HIV-1 in semen after treatment of urethritis: Implications for prevention of sexual transmission of HIV-1. Lancet. 1997; 349(9069):1868-1873.
20 Unemo M, Shafer WM. Antimicrobial resistance in Neisseria gonorrhoeae in the 21st Century: Past, evolution, and future. Clin Microbiol Rev. 2014; 27(3):587-613.
21 Crew PE, Abara WE, McCulley L et al. Disseminated gonococcal infections in patients receiving eculizumab: a case series. Clin Infect Dis. 2018 Nov 12.
22 Dudareva-Vizule S, Haar K, Sailer A et al. Prevalence of pharyngeal and rectal Chlamydia trachomatis and Neisseria gonorrhoeae infections among men who have sex with men in Germany. Sex Transm Infect. 2014; 90:46-51.
23 Buder S, Dudareva S, Jansen K et al. Antimicrobial resistance of Neisseria gonorrhoeae in Germany: low levels of cephalosporin resistance, but high azithromycin resistance. BMC Infect Dis. 2018 Jan 17;18(1):44.
24 Lewis DA. Will targeting oropharyngeal gonorrhoea delay the further emergence of drug-resistant Neisseria gonorrhoeae strains? Sex Transm Infect. 2015;91(4):234-7.
25 Serra-Pladevall J, Caballero E, Roig G et al. Comparison between conventional culture and NAATs for the microbiological diagnosis in gonococcal infection. Diagn Microbiol Infect. 2015; Dis. 83:341-3.
26 Ison CA, Golparian D, Saunders P et al. Evolution of Neisseria gonorrhoeae is a continuing challenge for molecular detection of gonorrhoea: false negative gonococcal porA mutants are spreading internationally. Sex Transm Infect. 2013; 89:197-201.
27 Unemo M, Dillon JA. Review and international recommendation of methods for typing neisseria gonorrhoeae isolates and their implications for improved knowledge of gonococcal epidemiology, treatment, and biology. Clin Microbiol Rev. 2011 Jul;24(3):447-58.
28 Wind CM, Schim van der Loeff MF, Unemo M et al. (2016) Test of Cure for Anogenital Gonorrhoea Using Modern RNA-Based and DNA-Based Nucleic Acid Amplification Tests: A Prospective Cohort Study. Clin Infect Dis. 2016; 62:1348-55.
29 AWMF (2019), angemeldete Leitlinie: Diagnostik und Therapie der Gonorrhoe, Registriernummer 059-004 https://www.awmf.org/leitlinien/detail/anmeldung/1/ll/059-004.html, zuletzt geprüft am 17.01.2019.











 Diese Seite weiter empfehlen
Diese Seite weiter empfehlen
