The Liver Meeting, 8.-12. November 2019, Boston
 Neues zu Hepatitis C und B
Neues zu Hepatitis C und B
Der Nutzen der Heilung der chronischen Hepatitis C steht mittlerweile (zumindest bei Klinikern) außer Frage. Es sinkt nicht nur die Leber-assoziierte Mortalität, auch auf kardiovaskuläre Ereignisse und Niereninsuffizienz hat die Heilung einen günstigen Einfluss (Butt A et al., 0039; Li J et al., 0037). Die Frage, ob DAA die Entstehung eines hepatozellulären Karzinoms (HCC) fördern, ist ebenfalls vom Tisch. Im Gegenteil, die Therapie der Hepatitis C senkt bei behandelbarem HCC das Mortalitätsrisiko um 63% (Dang H et al., 0040).
WHO-Ziel vor Augen
Die WHO hat 2016 dazu aufgerufen, die Hepatitis C weltweit zu eliminieren. Konkrete Ziele wurden formuliert: 80% weniger neue Hepatitis-B- und Hepatitis-C-Infektionen und eine Reduktion der Mortalität um 65% bis 2030. Berechnungen zeigen, dass es möglich ist, diese Ziele zu erreichen, doch bislang ist der Fortschritt in den Ländern sehr variabel. Auf dem amerikanischen Leberkongress haben nun die vier wichtigsten Lebergesellschaften, die American Association for the Study of Liver Disease (AASLD), die European Association for the Study of the Liver (EASL), die Latin American Association for the Study of the Liver (ALEH) und die Asian Pacific Association for the Study of the Liver (APASL) dazu aufgerufen, sich mehr zu engagieren. Die vier Gesellschaften sind eine Partnerschaft mit der Clinton Health Access Initiative eingegangen und haben vier Strategien entwickelt:
- Vereinfachung von Diagnostik und Therapiealgorithmus
- Integration der Hepatitis C Therapie in die medizinische Grundversorgung und andere Erkrankungsprogramme
- Dezentralisierung der HCV-Versorgung hin zu lokalen Ebenen
- Arbeitsteilung mit Ärzten in der Grundversorgung und anderen Gesundheitsdiensten.
Mittlerweile sei es möglich, HCV-Antikörper-Schnelltest und HCV-Nachweis im Blut während eines Besuchs durch-zuführen und die Therapie gleich mit einem der neuen pangenotypischen DAA einzuleiten. Die Effektivität der DAA-Therapie ist sehr gut und die Verträglichkeit ausgezeichnet; das belegen erneut Auswertungen der vielen „real world“ Kohorten.
G/P bei GT3
Die Bedeutung des Stadiums der Lebererkrankung für den Therapiealgorithmus bei Hepatitis C tritt bei therapienaiven Patienten (mit Ausnahme der dekompensierten Leberzirrhose) immer weiter in den Hintergrund. Bei Sofosbuvir/Velpatasvir (SOF/VEL) beträgt die Therapiedauer bei Patienten ohne Zirrhose/kompensierter Zirrhose 12 Wochen, bei Glecaprevir/Pibrentasvir (G/P) acht Wochen – laut europäischer Zulassung mit Ausnahme der Zirrhotiker Genotyp 3. Doch auch bei dieser Gruppe scheinen acht Wochen auszureichen. In der Studie EXPEDITION-8 haben 60/61 der GT3-Patienten (PP-Analyse) mit kompensierter Zirrhose die SVR12 erreicht (Abb. 1). Lediglich ein Patient hatte einen Relaps. Alle Patienten mit A30K oder Y93H bei Therapiebeginn wurden geheilt (Brown RS et al., LP9).
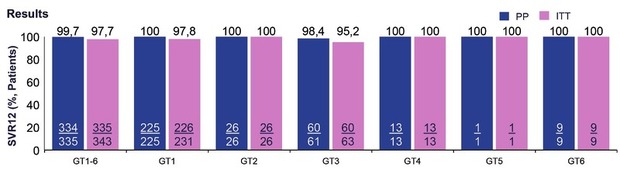
Abb. 1 Studie EXPEDITION-8. Glecaprevir/Pibrentasvir 8 Wochen bei therapienaiven Patienten mit GT1-6 und kompensierter Zirrhose. Ein Patient mit GT3a hatte Relaps zu Woche 4 nach Therapieende
Brown RS et al., 2019
Retherapie
Die wenigen Versager einer DAA-Therapie haben bei einer Retherapie eine sehr gute Aussicht auf Heilung. Am zuverlässigsten ist die Retherapie mit Sofosbuvir/Velpatasvir/Voxiplaprevir (SOF/VEL/VOX), besser als eine erneute Therapie mit SOF/VEL oder G/P selbst bei längerer Therapiedauer. Beim Vergleich der Retherapie nach Versagen unterschiedlicher DAA-Regime wurden nicht geheilt: 8/55 Patienten durch G/P (16-8 Wochen) und 3/176 durch SOF/VEL/VOX (12 Wochen). Alle versagenden Patienten hatten GT1a – mit einer Ausnahme GT1b (Flamm SL et al., 1500). Auch in einer Studie, in der 44/90 Patienten nach Versagen von G/P (meist GT3a, 60% NS5A-RAS, 16% NS3-RAS) erneut behandelt wurden, wurden 41/41 durch SOF/VEL/VOX geheilt, aber nur 2/3 durch SOF/VEL (Garcia F et al., 1658). Prädiktoren für ein Versagen von SOF/VEL/VOX scheint eine Leberzirrhose und/oder eine Vortherapie mit SOF/VEL zu sein. Im kanadischen Register wurden nach Versagen von SOF/VEL mit 2-Klassen-RAS drei Patienten durch die Tripletherapie nicht geheilt im Vergleich zu allen Patienten nach Versagen anderer DAA-Regime (Onofrio F et al., 1631).
Drogengebraucher
Um die Hepatitis C in der westlichen Welt zu eliminieren, müssen vor allem Drogengebraucher und MSM behandelt werden. Diese Gruppen haben eine hohe HCV-Prävalenz und ein hohes Reinfektionsrisiko. In den USA versuchte man, die Therapie niedrigschwellig anzubieten durch Verlagerung von spezialisierten Ärzten auf geschulte Primärärzte. In diesem Setting erreichte man bei 91% der Drogengebraucher eine SVR (modifizierte ITT-Analyse), doch Therapieunterbrechungen waren häufig und verminderten die SVR-Rate auf 78% (Dhiman RK et al., 0165). Problematisch sind auch die 3mal höheren Reinfektionsraten der IV-Drogengebraucher im Vergleich zu Menschen ohne Drogen (Janjua N et al., 0282).
Akute Hepatitis C
Ein wesentlicher Baustein zur Eliminierung von HCV ist die frühe Behandlung bevor die Infektion weitergegeben werden kann, d.h. die Behandlung der akuten Hepatitis C. In der Interferon-Ära war das möglich, sogar mit einer verkürzten Therapiedauer. Ist das auch bei DAA-Therapie eine Option? Das untersuchte die REACT-Studie. In dieser Untersuchung wurden HCV-mono- und HIV/HCV-koinfizierte Patienten (n=167, 79% MSM, 33% HCV-Reinfektion) mit akuter Hepatitis C sechs Wochen bzw. 12 Wochen mit SOF/VEL behandelt. Die Studie wurde aufgrund der Unterlegenheit der kurzen Therapie in der Interimsanalyse vorzeitig beendet. In der ITT-Analyse erreichten 79% im 6-Wochen-Arm und 95% im 12-Wochen-Arm eine SVR12 (p=0,027). Einen Relapse erlitten sechs Patienten im Behandlungsarm mit 6-wöchiger Therapie und kein Patient im 12-Wochen-Arm (Abb. 2) (Matthews GV et al., LP2).
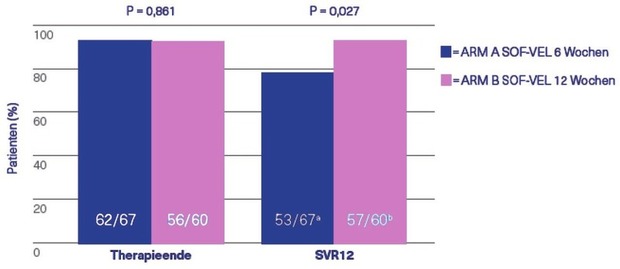
Abb. 2 Studie REACT. Sofosbuvir/Velpatasvir 6 vs. 8 Wochen bei akuter Hepatitis C. Interimanalyse. SVR-Raten zu Ende der Therapie und 12 Wochen später (SVR 12)
Matthews GV et al., 2019
Bald neue Definition
Die Möglichkeit einer Therapie der akuten Hepatitis C mit einem zugelassenen Medikament rückt damit in weite Ferne. Ein anderer Weg zu diesem Ziel könnte eine neue Definition der chronischen Hepatitis C sein. Bislang gilt die Infektion erst sechs Monate nach Ansteckung als chronisch. Die europäische AIDS Gesellschaft hat hier einen ersten Schritt getan und empfiehlt HIV/HCV-Koinfizierte zu behandeln, wenn die HCV-RNA innerhalb von vier Wochen nach Infektion nicht um mindestens 2 Logstufen abfällt bzw. wenn HCV-RNA nach 12 Wochen noch nachweisbar ist. Die Wahrscheinlichkeit einer spontanen Ausheilung ist dann sehr gering. Menschen mit hohem Transmissionsrisiko sollten, so die Empfehlung, sogar sofort behandelt werden. Eine Änderung der deutschen Leitlinien in dieselbe Richtung ist in Vorbereitung.
Organtransplantation
Seit einiger Zeit werden Organe von Spendern mit Hepatitis C transplantiert. Dabei kommt es regelhaft zur Infektion des Empfängers. Nach Transplantation einer HCV-positiven Leber ist das Virus innerhalb von fünf Tagen im Blut des Empfängers nachweisbar. Die Infektion kann dann jedoch sehr gut mit einem DAA-Standardregime behandelt werden (Wijarnpreecha K et al., 0003). Eine andere Option ist die prophylaktische DAA-Gabe über vier Wochen, was bei Nierentransplantation gut funktioniert (Durand C et al., 0042). Die Zugabe von Ezetimib könnte die Prophylaxedauer weiter verkürzen. Im Tierversuch blockiert der Cholesterinsenker Ezetimib den Eintritt von HCV in die Leberzelle. Aus diesem Grund erhielten in einer Pilotstudie (n=25) die Empfänger eines Organs (12 Lunge, 8 Herz) von einem HCV-positiven Spender Glecaprevir/Pibrentasvir plus 10 mg Ezetimib sechs bis 12 Stunden vor der Transplantation sowie über sieben Tage nachher. Keiner der Patienten entwickelte eine chronische Hepatitis C. Eine transiente Virämie wurde bei 18/25 Empfängern während der HCV-Prophylaxe registriert, die allerdings nur bei neun Patienten quantifizierbar war (meist Genotyp 3) (Abb. 3) (Feld J et al.; 0038).
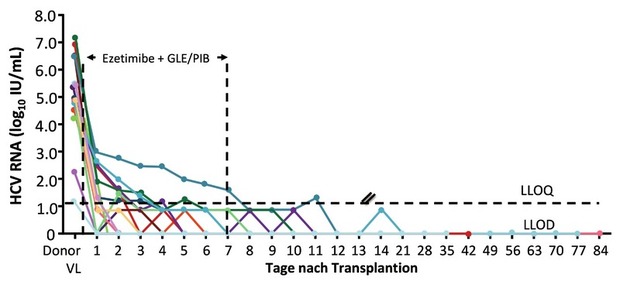
Abb. 3 Eezetimib plus Glecarevir/Pibrentasvir bei Transplantation HCV-positiver Organe. Virusverlauf bei HCV-negativen Empfängern
Feld J et al., 0038
Hepatitis B
Das Risiko einer HCC-Entwicklung ist unter Tenofovir und Entecavir nicht unterschiedlich. Die Analyse von zwei europäischen Kohorten (n=4.000, Beobachtungszeit 45 Monate bis 10 Jahre) widerspricht einer chinesischen Untersuchung, die auf dem europäischen Leberkongress im Frühjahr für viel Wirbel gesorgt hatte (Pol S et al., 0197; Papatheodoridis GV et al., 0454). Dafür haben chinesische Autoren jetzt ein vermindertes HCC-Risiko bei supprimierten Patienten mit gleichzeitiger Einnahme von Plättchenhemmern gefunden (Yip TCF et al., 0934).
Add-on Interferon?
Was bringt die Gabe von Interferon bei erfolgreicher Nukleosid-Therapie? Die Antwort der SWAP-Studie: Interferon erhöht die Wahrscheinlichkeit der immunologischen Kontrolle. In SWAP (n=253) wurden supprimierte Patienten entweder mit ihrem Polymerasehemmer weiterbehandelt oder 48 Wochen lang nur mit pegyliertem Interferon oder zusätzlich 48 Wochen mit Interferon. Nach 72 Wochen hatten mehr Patienten in den Interferon-Gruppen HBsAg verloren. Unter Interferon allein kam es selbst bei höheren HBsAg-Spiegeln bei mehr Patienten zum HBsAg-Verlust, allerdings mussten deutlich mehr Patienten dann schließlich doch ein Nukleosid erhalten (Abb. 4) (Lim SG et al., 0193).
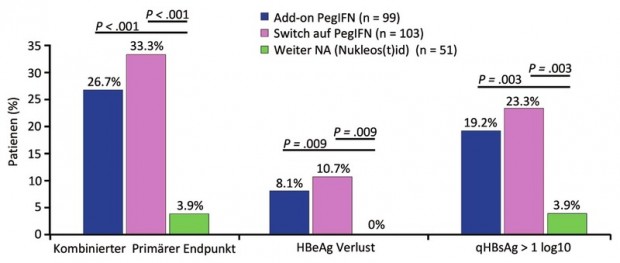
Abb. 4 Nukleos(t)id plus pegIFN vs. Switch auf pegIFN vs. Nukleos(t)id allein. Primäre Endpunkte zu Woche 72
Lim et al., 193
Heilung weit entfernt
Auf dem Weg zur funktionellen Heilung werden mehrere Wirkansätze allein und in Kombination geprüft: Hemmung der viralen Replikation, Reduktion der Antigenbildung und Stimulation der Immunabwehr. Der CAM (Core Assembly Modulator) JNJ-0440 senkt die HBV-DNA innerhalb von 29 Tagen um -3,2 log10 IU/ml (Gane E et al., 0089). Das Nukleotid GSK3389404 und der TLR8-Agonist GS-9688 vermindern die HBsAg-Spiegel bei Nuke-behandelten Patienten (Yuen et al., 0695, Gane E et al., 0697). Das Immunstimulans NASVAC, das nasal appliziert wird und sowohl HBs- als auch HBc-Antigen enthält, wird für die präventive und therapeutische Anwendung entwickelt. Behandelte (n=29) und unbehandelte (n=42) Patienten mit normalen Leberwerten erhielten die Vakzine alle zwei Wochen insgesamt 10 Mal. Die HBV-DNA bei den Unbehandelten fiel nicht signifikant um 10%. Der HBsAg-Spiegel ging bei zwei Drittel der Patienten zurück und zwar im Schnitt um rund 17%. Zwei Patienten verloren HBsAg (Yoshida O et al., 0088). Erstmals wurde auch eine HBV-Tripletherapie beim Menschen getestet. Die Kombination RNAi plus CAM plus Nukleosid war gut verträglich und führte zu einem deutlichen Abfall der HBsAg-Spiegel (Yuen MF et al., LP4).











 Diese Seite weiter empfehlen
Diese Seite weiter empfehlen
