The International Liver Congress, 13.-17. April 2016
Es kommt noch besser!
Real World
Die Zulassung der ersten Interferon-freien DAA-Regime gegen Hepatitis C beruhte auf Studien mit geringen Patientenzahlen. Daten aus dem klinischen Alltag sind daher besonders interessant. Erfreulicherweise bestätigen nahezu alle Kohorten und Register die gute Wirksamkeit und Verträglichkeit. Ein Vergleich der Regime anhand der zum Teil unterschiedlichen SVR-Raten ist nicht zulässig, da die Patientenkollektive in den Datensammlungen sehr verschieden sein können. So geht die im Vergleich niedrigere SVR-Rate bei Simeprevir/Sofosbuvir insbesondere in den frühen Kohorten vermutlich darauf zurück, dass diese Kombination das erste zugelassene Interferon-freie Regime war und deshalb mehr Patienten mit weit fortgeschrittener Lebererkrankung behandelt wurden.
Deutsches Register
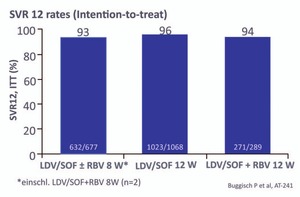
Abb.1 Deutsches Hepatitis C Register. SOF/LDV bei GT1 oder 4
Erstmals wurden jetzt auch Auswertungen des großen Deutschen Hepatitis C-Registers (DHC-R) präsentiert. Mit Ledipasvir/Sofosbuvir wurden rund 2.000 Patienten mit GT 1 oder 4 behandelt. Die SVR-Raten lagen bei 93% bei einer Therapiedauer von 8 Wochen, bei 96% bei 12 Wochen und bei 94% bei 12 Wochen plus Ribavirin. Alle Patienten, die 8 Wochen behandelt wurden, hatten zu Beginn eine HCV-RNA <6 Mio IU/ml. 2/9 Relapser bei Therapieverkürzung hatten eine Zirrhose (Abb. 1) (Buggisch P et al., SAT-241). Die Bedeutung von Protonenpumpenhemmer wurde im DHC-R nicht ausgewertet. In der amerikanischen TRIO-Kohorte hatten Säureblocker keinen negativen Einfluss auf die Heilung – außer, wenn der PPI zweimal täglich eingenommen wurde (SVR 98% vs 91%) (Afdhal N et al., LBP519).
3D-Regime überzeugt
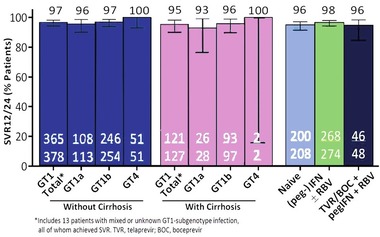
Abb. 2 Deutsches Hepatitis C Register. 3D/2D bei GT1 oder 4
Über 1.000 Patienten mit GT 1 oder 4 erhielten das 3D- bzw. 2D-Regime. 96% wurden geheilt (GT1a 95%, GT1b 97%, GT4 100%). Alle Patientengruppen hatten gut angesprochen, auch Drogen-abhängige, Patienten mit eingeschränkter Nierenfunktion/Dialyse und Zirrhotiker (Abb. 2). 22% der Patienten hatten eine Zirrhose, 7% davon waren im Stadium CP B/C. Nur sechs Patienten hatten einen Relaps und nur einer davon hatte eine Zirrhose. Schwere Nebenwirkungen waren sehr selten – selbst bei Zirrhose (4%). Ein interessanter Nebenbefund der Studie: 24%-11% der Patienten wurden nicht entsprechend dem Zulassungstext behandelt. Sie schnitten etwas schlechter ab (SVR 92% vs 99%) (Hinrichsen H et al., GS07). RAVs zu Baseline hatten keinen Einfluss auf das Therapieergebnis (Sarrazin C et al., LBP503).
Enttäuschung bei GT2
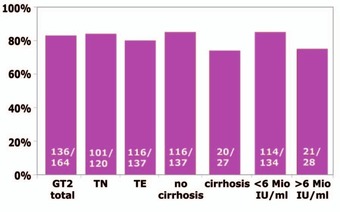
Abb. 3 SVR12 ITT (SOF+RBV 12 Wochen) in GT2
Anders sieht das Bild bei GT2 aus. Das derzeit von den Leitlinien favorisierte Regime Sofosbuvir/Ribavirin hat im DHC-R nur 83% der 164 Patienten geheilt. Besonders schlecht waren die SVR-Raten bei Zirrhotiker (74%) und Patienten mit hoher Viruslast (>6 Mio IU/ml 7%) (Abb. 3) (Tacke F et al., SAT-155). Der Grund für das schlechte Ergebnis ist derzeit unklar. Die Bedeutung der sogenannten St. Petersburg-Variante, ein chimäres Virus aus GT1 und GT2, das in herkömmlichen Tests als GT2 identifiziert wird, soll noch untersucht werden.
Sorgenkind GT3
Patienten mit GT 3 wurden im DHC-R mit vielen unterschiedlichen Regimen behandelt. Mit Sofosbuvir/Ribavirin über 24 Wochen wurden nur 73% der Zirrhotiker geheilt. Ledipasvir/Sofosbuvir/Ribavirin 24 Wochen führte bei 97% zur Heilung. Am besten war bei diesen schwer zu heilenden Patienten Daclatasvir/Sofosbuvir/Ribavirin 24 Wochen mit einer SVR von 97% (Cornberg M et al., SAT-208). Erfreulicherweise sind bei GT3 weitere Optionen in Sicht – allerdings frühestens Ende 2017.
Point of no return
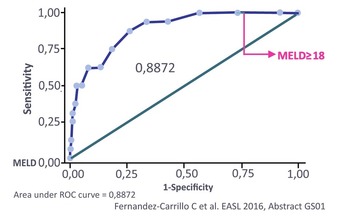
Abb. 4 HEPA-C Register. Ab MELD ≥18 überwiegt das Risiko den Nutzen der Therapie
Der Nutzen der SVR insbesondere bei fortgeschrittener Leberzirrhose wird immer wieder diskutiert. In Studien an Zirrhotikern im Stadium B oder C hatten sich viele Patienten verbessert, einige jedoch verschlechtert, was die Frage nach einem „Point of no return“ aufwirft. In zwei Kohorten wurden nun Nutzen und Risiko der Therapie bei diesen schwer kranken Patienten verglichen. Im spanischen HEPA-C Register lag die SVR bei CPT A bei 94%, bei CPT B/C bei 78% und schwere Nebenwirkungen wurden bei 12% vs 50% beobachtet. Als Cut-off für eine günstige Nutzen-Risiko-Relation für die Therapie wurde ein MELD <18 errechnet (Abb. 4) (Fernandez-Carrillo C et al., GS01). In einem englischen Register lag der Cut-off bei einem MELD <15 (Cheung et al., PS097).
Intensiv diskutiert wurde auch die Frage, ob DAA das Risiko von hepatozellulären Karzinomen (HCC) erhöhten. In einer retrospektiven Analyse wurden die Daten von 344 Zirrhotikern mit CP B/C ausgewertet. Alle wurden behandelt und 12-14 Wochen nachbeobachtet. Die SVR betrug 89%. HCCs traten insgesamt bei 7,6% der Patienten auf, bei Patienten mit vorherigem HCC bei 29% , was deutlich über der zu erwartenden Rate liegt (Buonfiglioli F et al., LBP506).
Vor der Tür
Kurz vor der Zulassung stehen zwei neue Fixkombinationen: Elbasvir/Grazoprevir und Sofosbuvir/Velpatasvir. Die großen Zulassungsstudien für die neuen Präparate wurden bereits auf dem amerikanischen Leberkongress vorgestellt. Die MSD-Kombination aus einem Proteasehemmer und NS5A-Hemmer wurde an einem breiten Patientenkollektiv geprüft und kann auch bei stark eingeschränkter Nierenfunktion/Dialyse eingesetzt werden. Sie ist in den USA bereits zugelassen gegen GT1 und 4. Auf dem EASL wurde C-EDGE vorgestellt, ein Vergleich von ELB/GZP gegen Sofosbuvir in Kombination mit pegIFN/RBV bei 225 Patienten mit GT1 oder 4. Das Interferon-freie Regime war signifikant überlegen – sowohl im Hinblick auf die Wirksamkeit als auch auf die Verträglichkeit und Sicherheit (Sperl J et al., PS002).
Zu Sofosbuvir/Velpatasvir wurde ASTRAL-5 präsentiert. In dieser Studie wurden 106 HIV/HCV-Koinfizierte mit GT 1-4 behandelt. Die SVR-Raten lagen bei 92-100% (Wyles P et al., PS104).
Akute Hepatitis C
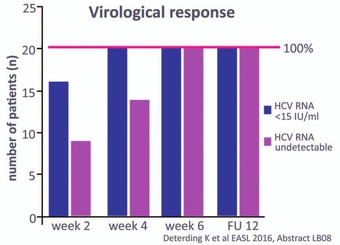
Abb. 5 Therapie der akuten symptomatischen Hepatitis C. SVR nach 6 Wochen LDV/SOF
Die SVR-Rate bei akuter Hepatitis C nach 6 Wochen Ledipasvir/Sofosbuvir lag in einer deutschen Multicenter-Studie bei 100% (Abb. 5). An der Studie hatten 20 Monoinfizierte mit GT 1a/b teilgenommen. Die Patienten waren rasch nach Diagnose behandelt worden, was es schwierig macht, den Einfluss einer potentiellen Spontanheilung abzugrenzen (Deterding K et al., LB08).
In 55% war eine sexuelle Transmission Ursache der Hepatitis C. Reinfektionen nach Hepatitis C-Therapie sind insbesondere bei HIV-positiven MSM häufig. In der europäischen NEAT-Kohorte hatten sich 25% der geheilten Patienten erneut infiziert. Das Risiko einer zweiten Reinfektion war sogar noch höher als das der ersten Reinfektion (Martin T et al., PS006). Eine Zulassungsstudie für die Indikation akute Hepatitis C ist jedoch leider nicht in Sicht.
Resistenz
Im klinischen Alltag spielen RAVs bei therapienaiven Patienten keine Rolle. In der amerikanischen HCV-TARGET Kohorte waren RAVs häufig (NS3 45%, NS5A 13%, NS5B 8%, >2 Klassen 10%). Sie hatten jedoch den Erfolg einer Therapie mit Ledipasvir/Sofosbuvir oder Simeprevir/Sofosbuvir nicht beeinflusst. Lediglich die sehr seltene NS5A-RAV Y93 (4%) verminderte die SVR-Rate (96% vs 75%) (Wang GP et al., PS102). Beim 3D-Regime war keinerlei Einfluss von RAVs auf die Wirksamkeit festzustellen auch nicht bei Vorbehandelten oder Zirrhotikern (Sarrazin C et al., LBP503).
Ein klinisch relevanter Prädiktor sind RAVs lediglich bei vorbehandelten Patienten mit Genotyp 3. So erreichten nach 24 Wochen Sofosbuvir/Velpatasvir 97% der DAA-Versager mit GT1 und 91% mit GT2 die SVR, aber nur 76% derer mit GT3. RAVs waren bei allen Genotyen nachweisbar, aber eben nur bei GT3 ein Prädiktor für das Versagen der Retherapie (Gane E et al., PS024). Aus diesem Grund empfahlen die Experten auf dem Kongress, einen Resistenztest nur vor Retherapie bei GT3-Patienten mit Fib-rose/Zirrhose durchzuführen. Bei allen anderen Patienten sei weder vor der ersten Therapie noch bei Retherapie ein Resistenztest indiziert.
Neue Generation
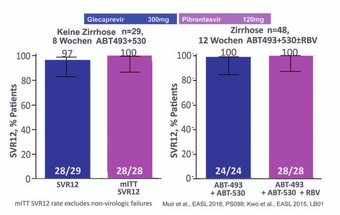
Abb. 6 12 Wochen Glecaprevir + Piprentasvir ± RBV bei GT3
Betrachtet
man den Erfolg der bisherigen DAA-Regime, fragt man sich, was kann da
noch verbessert werden? Die Latte hängt hoch angesichts der
ausgezeichneten Verträglichkeit und hohen SVR-Raten. Und doch, es
gibt noch Luft nach oben. Im Rennen ganz vorne sind Glecaprevir
(ABT493) + Piprentasvir (ABT530) von AbbVie und
Sofosbuvir/Velpatasvir + GS-9857 (Proteasehemmer) von Gilead gefolgt
von der Dreier-Kombination von MSD Grazoprevir + MK8408 + MK3682. Die
ersten beiden Regime führten in Phase-2-Studien zu SVR-Raten von
97-100% bei allen Genotypen, bei Zirrhotiker wie bei Vorbehandelten
mit RAVs.
Besonders
beeindruckend: 100% SVR nach
Glecaprevir + Piprentasvir 8 bzw. 12 Wochen bei GT3 ohne bzw. mit
Zirrhose ohne Ribavirin (Abb. 6) (Muir et al., PS098, Kwo PY et al.,
LB01).
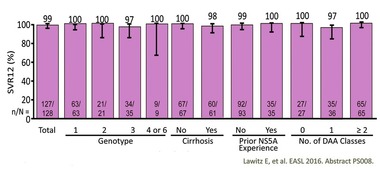
Abb. 7 SVR nach 12 Wochen SOF/VEL + GS9857 bei verschiedenen Subgruppen
99% SVR nach Sofosbuvir/Velpatasvir + GS-9857 nach DAA-Versagen bei allen Genotypen (Abb. 7) (Lawitz E et al., PS008). Eine Verkürzung der Therapie auf 8 Wochen bei naiven Patienten ohne Zirrhose scheint möglich zu sein. 6 Wochen waren zu kurz (Gane EJ et al., SAT-138).
Warten oder starten?
Angesichts dieser vielversprechenden Ergebnisse wird man sich fragen, bei welchen Patienten man auf die neuen Medikamente warten soll. Hier gilt es zu bedenken, dass es sich um Phase-2-Studien mit kleinen Patientenzahlen handelt, die erst bestätigt werden müssen. Dennoch kann man sagen, dass für die heute schwer zu behandelnden Patienten in absehbarer Zukunft bessere Optionen in Sicht sind.
Und in ferner Zukunft warten möglicherweise noch weitere Verbesserungen. 40/41 Patienten konnten mit einer subkutanen Injektion von mir122-Inhibitor RG-101, gefolgt von 4 Wochen Daclatasvir bzw. Simeprevir bzw. LDV/SOF und einer weiteren RG-101 Injektion geheilt werden (Horvath G et al., GS208).
Hepatitis B
Generische DAA funktionieren auch!
In Deutschland haben wir das Glück, alle Patienten mit Hepatitis C behandeln zu können. In vielen Ländern ist das nicht so – sei es, weil es eine Priorisierung für fortgeschrittene Lebererkrankungen gibt oder weil es die finanziellen Ressourcen eines Landes grundsätzlich nicht erlauben. Hier will der australische HepC Buyer´s Club (www.fixhepc.com) weiterhelfen. Die Organisation stellt Informationen zum legalen Import von Generika von renommierten Herstellern zur Verfügung. Gleichzeitig rät sie, die Therapie nur unter ärztlicher Aufsicht durchzuführen. Dass die Behandlung auch mit Generika funktioniert, belegt eine von der Gruppe organisierte internationale Studie. 139 Patienten wurden entweder mit generischen DAA aus Indien oder China oder mit Originalpräparaten behandelt. Die SVR-Raten waren vergleichbar (Freeman J et al., LB03).
Wie immer stand die Hepatitis B im Schatten. Besonders interessant sind die Ansätze zur Heilung der Hepatitis B.
Es sind viele Substanzen mit unterschiedlichen Wirkmechanismen in der Pipeline. Der Entryinhibitor Myrcludex B hat in Kombination mit Tenofovir in einer Phase-1-Studie die HBV-DNA um 1,7 log vermindert (Blank A et al., PS054). Der siRNA-Inhibitor ARC-520 führte in einer Phase-2-Studie bei HBeAg-positiven Patienten zu einem Abfall von HBsAg, nicht so jedoch bei HBe-Ag-Negativen (Yuen M-F et al., THU-193). Und der erste Core- oder Kapsid-Inhibitor NVR-3-778 senkte die HBV-DNA in einer ersten Studie am Menschen um 1,7 log (Yuen M-F et al., LB06).
TAF für Hepatitis B
Die neue Tenofovir-Form Tenofovir Alafenamid wurde bei der chronischen Hepatitis B geprüft. Die Wirkung der alten und neuen Formulierung ist bei HBeAg-positiven wie -negativen Patienten vergleichbar (Buti M et al., #GS06; Chan Henry YJ et al., #GS12). Die Zulassung wird vermutlich noch in diesem Jahr erfolgen. 2017 läuft das Patent für das herkömmliche Tenofovir Diproxil aus. Man darf gespannt sein, was dann schwerer wiegt, der günstigere Preis von Tenofovir Diproxil oder die Vorteile der neuen Formulierung.










 Diese Seite weiter empfehlen
Diese Seite weiter empfehlen
